题目内容
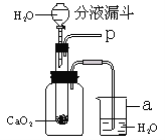
【题目】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
(猜想)ⅠCuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
ⅡCuO参与反应产生O2,反应前后质量和化学性质发生了改变;
ⅢCuO是反应的催化剂,反应前后__________________.
(实验)用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
____________带火星的木条复燃. | ________ | 溶液中有气泡放出, ___________ | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立. |
(2)步骤①的目的是_____________________.
(3)过氧化氢能被CuO催化分解放出O2的文字表达式为________________,其中CuO对反应生成的氧气的多少________(填“有”或“无”)影响。
【答案】质量和化学性质不变 溶液中有气泡放出 固体质量仍为0.2g 带火星的木条复燃 与步骤③对比,检验加入CuO前后双氧水分解速度有无变化 过氧化氢![]() 水+氧气 无
水+氧气 无
【解析】
Ⅲ.催化剂的特点是“一变,两不变”,即反应速率变,质量和化学性质不变;
(1)氧化铜对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,步骤③现象现象是有气泡,带火星的木条复燃;催化剂的特点是“一变,两不变”,反应前后其质量不变,所以氧化铜的质量仍为0.2g;催化剂的特点是“一变,两不变”,其中反应速率改变,这里是加快,所以现象是溶液中有气泡放出,带火星的木条复燃;
(2)为了看氧化铜是否能改变反应的速率,要通过加入氧化铜与不加氧化铜的现象进行对比,才能得出科学合理的结论;
(3)双氧水反应生成水和氧气,过氧化氢能被CuO催化分解放出O2的文字表达式是过氧化氢![]() 水+氧气。CuO是催化剂,对反应生成的氧气的多少无影响。
水+氧气。CuO是催化剂,对反应生成的氧气的多少无影响。

 星级口算天天练系列答案
星级口算天天练系列答案【题目】某石油化工厂化验室的实验员用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,测得实验数据如下表所示。
实验序号 | 消耗NaOH溶液的质量 | 洗涤后溶液的pH |
① | 30g | pH<7 |
② | 40g | pH=7 |
③ | 50g | pH>7 |
若一定量石油产品中残余硫酸的质量为100 g,请计算该残余硫酸的溶质质量分数(写出详细的计算过程)。__________