题目内容
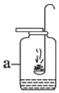
【题目】小强取一条长10cm、宽1cm的滤纸条,在滤纸条上每隔1.5-2cm处滴一小滴酚酞溶液,滴好后把滤纸条放到试管里,在试管口塞一团棉花.塞好后放在实验桌上(如图所示),用滴管吸取浓氨水,在试管口的棉花上滴10~15滴。
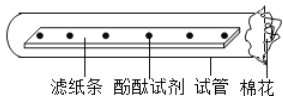
(1)观察到的现象是_______________________________,说明_________________________.
(2)小强同学做此实验时,发现滤纸条上没有变色,而试管中所塞的棉花却变成了红色.导致这种现象产生的错误操作可能是_____________________________,这一实验还说明,两种试剂中________________具有挥发性.
(3)为什么湿衣服在阳光照射下更容易变干______________________________.
【答案】 滤纸条上的酚酞从外向里逐渐变红 分子不断运动 氨水滴到滤纸上,酚酞溶液滴到了棉花上 浓氨水 在阳光下,温度高,水分子运动速率加快
【解析】(1)由于分子在不断运动,氨水具有挥发性,运动速度加快,运动到与酚酞试液接触,由于氨水属于碱,能使酚酞试液变红色;所以滤纸条上滴加酚酞试液的点由试管口向内依次变红,该实验说明了分子在不断运动;(2)由于氨水属于碱,能使酚酞试液变红色,试管内滤纸条上没有变化,而试管口塞的 棉花却变成红色说明氨水滴到了滤纸上,酚酞溶液滴到了棉花团上。这一实验还说明,两种试剂中氨水具有挥发性;(3)由于分子是运动的,温度高运动的速率加快。所以,湿衣服在阳光照射下更容易变干。

 单元期中期末卷系列答案
单元期中期末卷系列答案【题目】小明对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想假设】a. 可能与硫酸的浓度(质量分数)有关; b.可能与锌的形状有关。
【设计实验】小明用不同质量分数的硫酸和不同形状的锌进行如下实验。
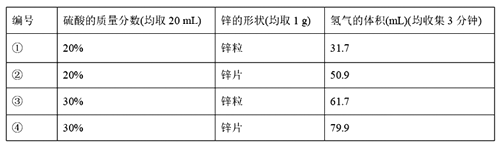
【收集证据】要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是__________。
【得出结论】通过③、④可以获得的结论是______________________________________。
【交流反思】
(1) 下表是小明第①组实验的详细数据。
H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
请你解释一段时间后,锌与硫酸反应由快变慢的变化原因:___________________________。
(2) 锌与硫酸反应的快慢可能还受___________________因素影响。(填一种)
【题目】一些金属易生锈,某小组同学设计如下实验,对金属锈蚀进行探究.
【实验一】取5枚去油去锈的洁净铁钉,分别装入下表的试管中,进行实验.
实验图示 |
|
|
|
|
|
生锈时间 | 8min | 较长时间不生锈 | 5min | 3min | 1min |
(1)通过上述实验可知,温度越高铁钉生锈速率越____(填“慢”或“快”);在_____(填“酸性”、“碱性”或“中性”)环境中铁钉生锈速率较快.
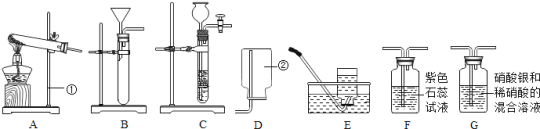
【实验二】为探究铁锈的成分,用图1所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全).
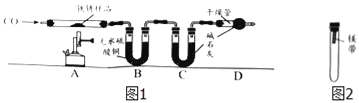
【查阅资料】无水硫酸铜能吸收水而变蓝,碱石灰既能吸收水也能吸收CO2.
(2)请指出图1所示实验装置的一个明显缺陷:___________________.
(3)加热前,先通入CO一段时间,目的是____________________.
(4)将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,由此推知铁锈中一定含有_____元素,从而推断出空气中的_______参加了铁生锈反应.
【实验记录】
铁锈样品的质量/g | 装置B的质量/g | 装置C的质量/g | |
反应前 | 23.2 | 232.4 | 198.2 |
反应后 | / | 239.6 | 211.4 |
(5)根据上表数据推算,可确定铁锈的成分,用FexOynH2O表示,则n=_______;若缺少D装置,x:y的值_________(填“偏大”、“偏小”或“无影响”).
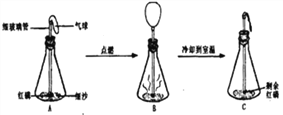
(6)欲通过实验探究镁带在空气中锈蚀的条件,用图2所示装置,试管内可选用的物质如下:
①O2 ②水 ③CO2 ④O2和CO2 ⑤CO2和水 ⑥O2和水 ⑦O2、CO2和水
至少需要选用___________(填数字序号),才能达到探究镁带锈蚀的条件.
(7)请写出镁带在空气中锈蚀,生成碱式碳酸镁[Mg3(OH)2(CO3)2]的化学方程式_______.