题目内容
【题目】归纳推理是学习化学重要的方法,必须严谨、科学,下列归纳推理正确的是![]()
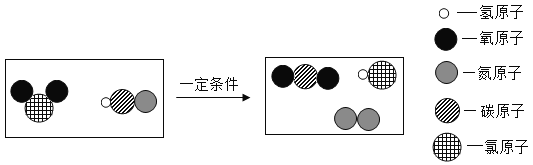
A.一定条件下,C能够还原![]() 生成Fe,所以C也能够还原CuO生成Cu
生成Fe,所以C也能够还原CuO生成Cu
B.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
C.溶液是均一的、稳定的,所以均一的、稳定的液体一定是溶液
D.原子核是由质子和中子构成的,所以所有的原子都有质子和中子
【答案】A
【解析】
A、碳具有还原性,一定条件下,C能够还原![]() 生成Fe,所以C也能够还原CuO生成Cu,选项推理正确;
生成Fe,所以C也能够还原CuO生成Cu,选项推理正确;
B、中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如![]() ,选项推理错误;
,选项推理错误;
C、溶液是均一的、稳定的,但均一的、稳定的液体不一定是溶液,如水,选项推理错误;
D、原子核是由质子和中子构成的,并不是所有的原子都有质子和中子,如氢原子中没有中子,选项推理错误。故选A。

【题目】(8分)常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
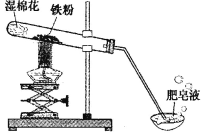
(1)试管尾部放一团湿棉花的目的是_______________。
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。 说明生成的气体是______________。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_____________。
【实验探究】
实验操作 | 实验现象及结论 |
【实验结论】铁和水蒸气反应的化学方程式为___________________________________。
【反思与交流】该黑色固体不可能是Fe2O3,理由是_______________________________。
【题目】酸、碱、盐是初中化学学习的重要知识。根据所学知识,某化学兴趣小组设计了如下两个实验,探究氢氧化钠与二氧化碳的反应。
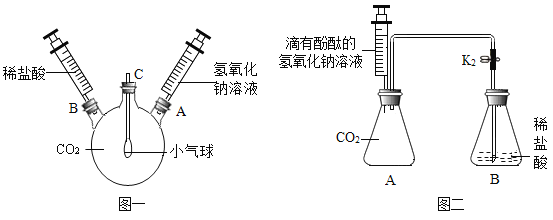
(1)如图一装置所示,先将氢氧化钠溶液注入三颈烧瓶中,然后再将稀盐酸注入三颈烧瓶中,观察到气球的变化是________________,产生这一现象的原因是_______________。
(2)根据实验一的原理,兴趣小组的同学又设计了图二装置。实验前关闭K,先将注射器中的氢氧化钠溶液注入A中,然后再打开K,稀盐酸倒流进A中,片刻后停止倒流,A中溶液仍为红色。同学们对反应后A装置中的溶液成分产生了兴趣,提出了如下猜想:
猜想一: NaCl、 Na2CO3
猜想二: NaCl、 NaOH
猜想三: NaCl、NaOH、Na2CO3
①上述猜想不合理的是___________,原因是______。
同学们经过讨论设计了如下实验方案进行探究
实验操作 | 实验现象 | 实验结论或化学方程式 |
②__________________ | 有白色沉淀产生 | ③反应的化学方程式__________ |
静置,取上层清液,向其中滴加酚酞溶液 | ④_________________ | 猜想三成立 |
(3)上述实验结束后,兴趣小组的同学想将溶液的溶质都变为NaCl。他们向装置A中加入20g溶质质量分数为7.3%稀盐酸,恰好使红色完全退去,试计算反应后NaCl的质量增加了_______?