题目内容
【题目】A、B、C三种物质的溶解度曲线如图所示,请回答下列问题:
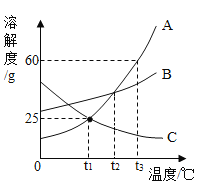
(1)t2℃时,A、B、C三种物质溶解度的大小关系是_____(用“A、B、C”和“>、<、=”表示)
(2)要使接近饱和的C溶液在保持溶质质量分数不变的情况下变成饱和溶液的方法是_____。
(3)将100g质量分数为30%的A溶液由t3℃降温至t1℃,降温后所得溶液中溶质的质量分数是_____。
(4)t3℃时,A、B、C三种物质的混合溶液中,A、B、C三种溶质的质量相等,将混合溶液在该温度下恒温蒸发溶剂,首先析出的物质是_____。
【答案】A=B>C 升高温度 20% C
【解析】
根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
(1)据图可以看出,在t2℃时,A、B、C三种物质的溶解度由小到大的顺序为A=B>C,故填:A=B>C;
(2)C的溶解度随温度的升高而减小,要使接近饱和的C溶液在保持溶质质量分数不变的情况下变成饱和溶液的方法是可用升高温度的方法,故填:升高温度;
(3)100g质量分数为30%的A溶液中A的质量为100g×30%=30g,水的质量为100g﹣30g=70g,t1℃A物质的溶解度为25g,则70g水中最多溶解A物质![]() ,故,降温后所得溶液中溶质的质量分数是
,故,降温后所得溶液中溶质的质量分数是![]() ,故填:20%;
,故填:20%;
(4)t3℃时,混合溶液中A、B、C三种溶质的质量相等,将混合溶液在该温度下恒温蒸发溶剂,溶解度小的物质先析出,故首先析出的物质是C。故填:C。

【题目】兴趣小组分析了用硫铁矿烧渣(主要成份Fe2O3、Fe3O4、FeO等)制备铁红(Fe2O3)的流程图并进行了铁红性质实验。铁红制备的流程图分析(注:NH4HCO3不稳定,易分解)
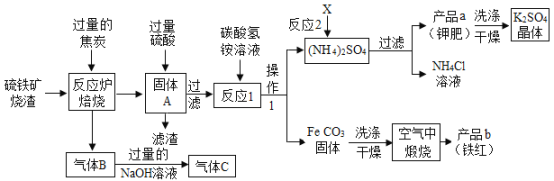
(1)写出焙烧中CO与Fe2O3反应的化学方程式_____。
(2)实验室完成操作1,用到的玻璃仪器有烧杯、玻璃棒和_____(填仪器名称)
(3)你认为对气体C最佳的处理方法是_____
A 冷却后排入空气 B 燃烧后排放 C 再通入反应炉
(4)反应1的反应温度一般需控制在35℃以下,其目的是_____。
(5)反应2中相关物质的溶解度如下表。你认为该反应在常温下能实现的原因是_____。
物质 | X | K2SO4 | NH4Cl | (NH4)2SO4 |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
洗涤干燥得到K2SO4晶体时,可选用下列_____(填字母)洗涤剂;
A KCl的饱和溶液 B 水 C K2SO4的饱和溶液