题目内容
【题目】兴趣小组分析了用硫铁矿烧渣(主要成份Fe2O3、Fe3O4、FeO等)制备铁红(Fe2O3)的流程图并进行了铁红性质实验。铁红制备的流程图分析(注:NH4HCO3不稳定,易分解)
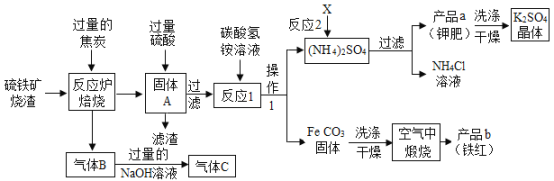
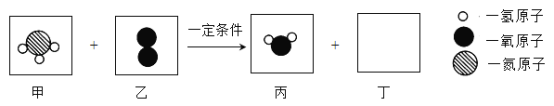
(1)写出焙烧中CO与Fe2O3反应的化学方程式_____。
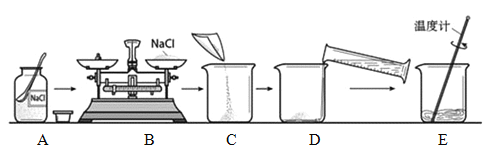
(2)实验室完成操作1,用到的玻璃仪器有烧杯、玻璃棒和_____(填仪器名称)
(3)你认为对气体C最佳的处理方法是_____
A 冷却后排入空气 B 燃烧后排放 C 再通入反应炉
(4)反应1的反应温度一般需控制在35℃以下,其目的是_____。
(5)反应2中相关物质的溶解度如下表。你认为该反应在常温下能实现的原因是_____。
物质 | X | K2SO4 | NH4Cl | (NH4)2SO4 |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
洗涤干燥得到K2SO4晶体时,可选用下列_____(填字母)洗涤剂;
A KCl的饱和溶液 B 水 C K2SO4的饱和溶液
【答案】Fe2O3+3CO![]() 2Fe+3CO2 漏斗 C 防止碳酸氢铵受热分解 常温下K2SO4的溶解度小 C
2Fe+3CO2 漏斗 C 防止碳酸氢铵受热分解 常温下K2SO4的溶解度小 C
【解析】
(1)焙烧中反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,反应条件是高温,反应的方程式是:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(2)将不溶于液体的固体和液体分离方法是过滤,过滤用到的玻璃仪器有:烧杯、玻璃棒、漏斗;
(3)反应炉中一氧化碳还原氧化铁生成铁和二氧化碳,过量的一氧化碳会随二氧化碳逸出,因此气体B为一氧化碳和二氧化碳的混合气体,通过足量的氢氧化钠溶液后,二氧化碳与氢氧化钠反应生成碳酸钠和水,因此气体C主要成分是一氧化碳,一氧化碳可作为还原剂重复利用。故选C;
(4)因为碳酸氢铵受热分解为氨气、水、二氧化碳,所以反应I的反应温度一般需控制在35℃以下,其目的是防止碳酸氢铵受热分解;
(5)根据复分解反应发生的条件,反应2中没有不溶物,但常温下硫酸钾的溶解度很小,在生成物中会以沉淀形式出现,所以反应可以发生,所以反应2在常温下能实现的原因是:常温下K2SO4的溶解度小,用硫酸钾饱和溶液清洗硫酸钾晶体,硫酸钾晶体不会减少,如果用水或其它溶液都会溶解一部分硫酸钾晶体。故选C。

【题目】为验证氢氧化钠的化学性质某兴趣小组同学做了如图所示实验。请根据实验回答问题
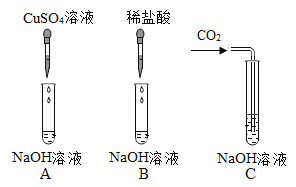
(1)A试管中观察到的实验现象是_____。
(2)甲同学观察到B试管中无明显现象,然后向B试管中继续滴加1~2滴无色酚酞溶液,振荡后溶液仍为无色。此现象_____(填“能”或“不能”)证明氢氧化钠溶液和稀盐酸发生了反应。
(3)为了验证C试管中有碳酸钠生成,乙同学设计的实验方案如表所示,请你帮助填写完整。
(查阅资料)碳酸钠溶液显碱性
方案 | 实验步骤 | 实验现象 | 反应的化学方程式 |
一 | ①取少量反应后溶液于另一支试管中 ②加入过量的稀盐酸 | _____ | _____ |
二 | ①_____ ②_____ | _____ | _____ |
【题目】化学课堂上,同学们在老师的指导下进行了分组实验。
(查阅资料)氯化钙溶液、氯化钠溶液都呈中性。
(1)第I组实验:探究酸和碱的反应。向试管中加入少量的氢氧化钙溶液,并滴入几滴无色酚酞溶液,充分振荡后,再逐滴滴入稀盐酸,并用玻璃棒不断搅拌,观察到溶液由红色变为无色,测得溶液的pH<7.该过程中发生反应的化学方程式为________,反应后溶液中的溶质为________。
(2)第Ⅱ组实验:为了探究一瓶忘记盖瓶塞的氢氧化钠溶液中溶质的成分,同学们进行了如下实验。
(提出猜想)
猜想1;溶质是氢氧化钠;
猜想2:溶质是________;
猜想3:溶质是碳酸钠。
(设计实验)
实验步骤 | 实验现象 | 实验结论 |
取少量样品于试管中,向其中加入适量的氯化钡溶液,充分反应后,过滤,向滤液中滴加几滴无色酚酞溶液 | ________ | 猜想3成立 发生反应的化学方程式为________。 |
(交流讨论)
老师问:“若向少量样品中,加入足量的稀盐酸,如果有气泡产生,猜想3一定成立吗?”同学们交流讨论后,一致认为猜想3不一定成立,原因是________。
(3)实验结束后,同学们将两组实验后的废液倒入同一个废液缸中进行集中处理。若使废液中只含有一种溶质氯化钠(酚酞除外)则需向废液中加入________。