��Ŀ����
����Ŀ��ij��ȤС������ͼװ�ã���ʯ���������ƺ����������ƵĻ�����������ˮ���������������������������װ������Ϊ16�ˣ��ⶨ����������Һ�����ʵ������������������������£�����װ��16�ˣ�


��ش�
��1��˫��ˮ��Ʒ�м���������̣�����������_____���ã���Ӧ�������������ʵ���Ϊ_____��
��2������ù���������Һ�����ʵ�����������_____��д��������̣�
��3��ʵ��װ������ƿ�ϼӽ�ʢ�м�ʯ�ҵĸ����������_____�����ʵ��װ���в���ʢ�м�ʯ�ҵĸ���ܣ���õĹ���������Һ���ʵ�����������ƫ��ԭ����_____��
���𰸡��� 0.025mol 2.5% ����װ���������ܵ�ˮ���� ���ʵ��װ���в���ʢ�м�ʯ�ҵĸ���ܣ�����װ����һЩˮ�����ܵ����������ٵĶ��ˣ���������������������ˣ�����������Ĺ�����������ƫ��õĹ���������Һ���ʵ�����������ƫ��
��������
����װ�õ������ļ����������������������������ڹ���������ˮ���������������ɢ���ϸ�����������գ��ٽ�һ�����з������ɡ�
�⣺��1��������������ý��������ã����������غ㶨�ɿ�֪��װ�õ������ļ���������������������������������������������84g+0.5g��83.7g��0.8g���������ʵ���Ϊ��![]() =0.025mol��
=0.025mol��
��2����Ҫ����0.8g������Ҫ�μӷ�Ӧ�Ĺ������������Ϊx����
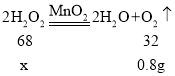
![]()
x=1.7g��
����������Һ����Ϊ��84g��16g��68g�����Թ���������Һ�����ʵ�����������![]() ��100%=2.5%��
��100%=2.5%��
��3��ʵ��װ������ƿ�ϼӽ�ʢ�м�ʯ�ҵĸ��������������װ���������ܵ�ˮ���������ʵ��װ���в���ʢ�м�ʯ�ҵĸ���ܣ������ʵ��װ���в���ʢ�м�ʯ�ҵĸ���ܣ�����װ����һЩˮ�����ܵ����������ٵĶ��ˣ���������������������ˣ�����������Ĺ�����������ƫ��õĹ���������Һ���ʵ�����������ƫ��

����Ŀ�������Ǽס���ʵ��С����ɵ����ʵ�顣
��С�飺������ͼװ���о�ȼ����������֪�����Ż��Ϊ40�棩��
������ձ���ʢ��80�����ˮ���ֱ���ȼ�ճ��ձ��е��ܿڷ���һС����ף�����ƿ����
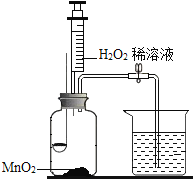
�������ע������ƿ����������H2O2 ��Һ
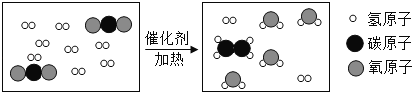
��1��H2O2ϡ��Һ��MnO2�Ӵ�ʱ������Ӧ�����ֱ���ʽΪ_____��
��2��ʵ���У�����H2O2��Һǰ��ȼ�ճ��еİ��ײ�ȼ�գ�ԭ����_____������H2O2��Һ�۲쵽�ձ��е�������_____��
��С�飺��Щ����Ӱ���������ֽ�����ʣ�
ʵ����� | H2O2�� ҺŨ��% | H2O2��Һ���/mL | �¶ȡ� | MnO2������/g | �ռ����������/mL | ��Ӧ���� ��ʱ��/s |
�� | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
�� | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
�� | 30 | 5 | 35 | 2 | 49.21 | |
�� | 30 | 5 | 55 | 2 | 10.76 |
��1��ͨ��ʵ��Աȿ�֪����ѧ��Ӧ������Ũ�Ⱥ��¶��й�ϵ��
��2����ѧ��Ӧ��ʵ������������Ӵ�����ײ�Ľ������ѧ��Ӧ��������������Ӵ�����ײ�ĸ����йء��Դ��۽ǶȽ��͡���Ӧ��Ũ��Խ��ѧ��Ӧ����Խ�족��ԭ���ǣ�_____��
��3����һ����15%�Ĺ���������Һ��������Ϊ�˼�С��Ӧ���ʣ��ɼ�������ˮϡ�ͣ�����������������_____�����С�����䡱��������