��Ŀ����
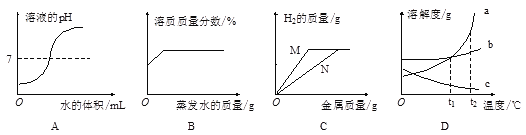
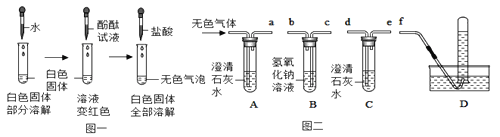
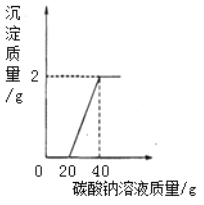
����Ŀ��ʵ��С���ͬѧ��ʵ������ȡ������̼��Ӧ�����Һ����������̽����ȡ����ʯ�����ᷴӦ�ҹ��˺����÷�Һ20�����ձ��У���ε���̼������Һ������������̼������Һ�����������ɳ����������ı仯��ϵ��ͼ��ʾ��
�Իش�
��1������ͼ����Ϣ��֪��20g��Һ�У������������� ��д��ѧʽ����
��2���ڷ�Һ�м���̼������Һ��������̼������Һ��Ӧ�Ļ�ѧ����ʽΪ ��
��3�������Һ���Ȼ��Ƶ����������Ƕ��٣�(д���������)
���𰸡���1��CaCl2��HCl
��2��Na2CO3+2HCl=2NaCl+ H2O +CO2��
��3��11.1%
��������̼��ƺ����ᷴӦ�ķ���ʽΪ�� CaCO3 +2HCl ==CaCl2+ CO2�� + H2O ����˿�֪��Ӧ�����Һ��һ�����Ȼ��ƣ��������Ȼ��⡣��ͼ��֪��ʼû���ɳ���˵����Һ�����������ʣ�Ϊ�Ȼ��ƺ��Ȼ��⣬��ʼ��������̼���ƺ����ᷴӦ���ɶ�����̼���Ȼ��ơ�ˮ�ķ�Ӧ������ʽΪNa2CO3+2HCl=2NaCl+ H2O +CO2�������Һ���Ȼ��Ƶ�����Ϊx,
CaCl2+Na2CO3=CaCO3��+2NaCl,
111 100
X 2g
111/x=100/2g
X=2.22g
��Һ���Ȼ��Ƶ�����������2.22g��20g��100%=11.1%

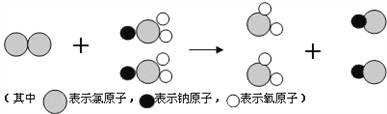
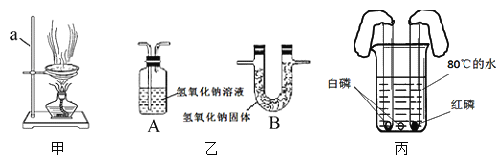
����Ŀ������ͼ�У� ��������ʾ���������ʼ���һ�������¿��Է�Ӧ�� ��������ʾ��һ�������¶�����ת��Ϊ�ҡ���������ѡ���з�������ͼҪ����ǣ� ��
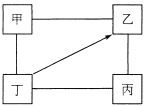
�� | �� | �� | �� | |
A | H2SO4 | Ba(NO3)2 | NaOH | Na2CO3 |
B | CaCl2 | K2CO3 | Ca(OH)2 | HCl |
C | C | H2O | CO2 | O2 |
D | Al | CuSO4 | Zn | H2SO4 |
A. A B. B C. C D. D