题目内容
【题目】CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl2·2H2O制备CuCl,并进行相关探究。
【资料查阅】
(1)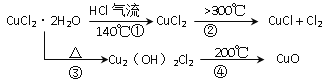
(2)Cl2是一种有毒气体,易溶于氢氧化钠溶液。
(3)HCl极易溶于水。
(4)CuCl常温下是固体,露置于空气中易被氧化为绿色的高价铜盐。
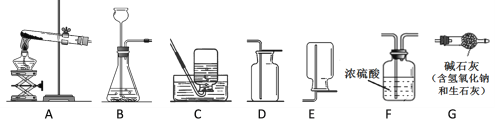
【实验探究】该小组用下图所示装置进行实验(夹持仪器已略)。
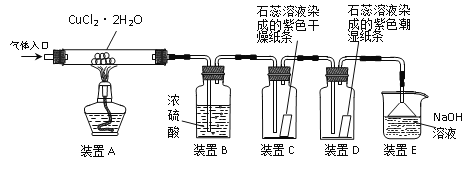
请回答下列问题:
(1)装置B的作用是_______________。装置E的作用是_______________。
(2)实验操作的先后顺序是a→_______________(填操作的编号)
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)检验该装置气密性的方法是_______________ 。
(4)在实验过程中,观察到C中纸条的颜色不变, 从微观角度分析氯化氢气体不显酸性的原因是_______________;D中纸条的先变红后褪色,其褪色的原因可能是_______________(填序号)。
A.氯化氢水溶液有漂白性 B.氯气的水溶液有漂白性
C.氯化氢气体有漂白性 D.干燥的氯气有漂白性
(5)停止通入HCl后,通入N2的目的是_______________ 。
(6)④中发生反应的化学反应方程式是________________ 。
(7)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是_______________。
②若杂质是CuO,则产生的原因是_______________。
【答案】 吸收水蒸气 吸收生成的氯气等 c d b e 在装置E上面的倒置漏斗换成导管,在烧杯中加少量水,将导管插入水中,在装置的气体入口处装上橡皮管,并用弹簧夹夹紧,用酒精灯微微加热玻璃管,若导管口有气泡冒出,则装置气密性良好 在氯化氢气体中,氯化氢是以分子形式存在的,没有解除离出氢离子,故氯化氢气体不显酸性 B 防上空气进入试管,把氯化亚铜氧化 Cu2(OH)2Cl2 ![]() 2CuO + 2HCl ↑ 加热时间不足或温度偏低 通入HCl的量不足
2CuO + 2HCl ↑ 加热时间不足或温度偏低 通入HCl的量不足
【解析】(1)根据浓硫酸和氢氧化钠的作用分析;
(2)根据实验步骤分析;
(3)根据检查装置气密性的方法分析;
(4)根据物质的构成及酸碱性分析;
(5)根据氮气的性质分析;
(6)根据图中的反应物、生成物、反应条件分析;
(7)根据加热的时间及通入HCl的量分析。
解:(1)装置B中装有浓硫酸,主要作用是吸收热分解CuCl2·2H2O制备CuCl时产生的水蒸气;装置E中装有氢氧化钠溶液,主要作用是吸收热分解CuCl2·2H2O制备CuCl时生成的氯气,防止污染空气;
(2)实验前先检查装置的气密性后加入药品,反应前需在“气体入口”处通入干燥HCl,除去空气避免对实验造成影响,然后点燃酒精灯,加热,反应结束后熄灭酒精灯,冷却,故实验操作的先后顺序是a→c→d→b→e;
(3)检验该装置气密性的方法是在装置E上面的倒置漏斗换成导管,在烧杯中加少量水,将导管插入水中,在装置的气体入口处装上橡皮管,并用弹簧夹夹紧,用酒精灯微微加热玻璃管,若导管口有气泡冒出,则装置气密性良好 ;
(4)在实验过程中,观察到C中纸条的颜色不变, 从微观角度分析氯化氢气体不显酸性的原因是在氯化氢气体中,氯化氢是以分子形式存在的,没有解除离出氢离子,故氯化氢气体不显酸性;D中纸条的先变红后褪色,其褪色的原因可能是氯气的水溶液中含有次氯酸具有漂白性;
(5)由于反应刚生成的氯化亚铜温度较高,易于空气中的氧气反应,故停止通入HCl后,通入N2的目的是防上空气进入试管,把氯化亚铜氧化;
(6)④中发生反应的化学反应方程式是Cu2(OH)2Cl2 ![]() 2CuO + 2HCl ↑;
2CuO + 2HCl ↑;
(7)①若杂质是CuCl2,则产生的原因是加热时间不足或温度偏低;
②若杂质是CuO,则产生的原因是通入HCl的量不足,部分CuCl2·2H2O反应最终生成了CuO。