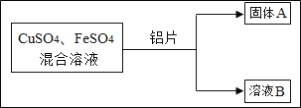
题目内容
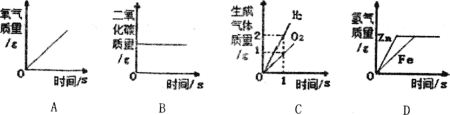
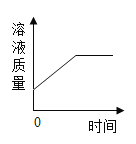
【题目】下列实验中所涉及物质的量的变化(不考虑水份蒸发)能用如图表示的是( )
A. 向一定量的硫酸铜溶液中加入足量镁粉
B. 向饱和的硝酸钾溶液中加入足量硝酸钾
C. 向一杯接近饱和的石灰水中加入少量氧化钙
D. 向一定量的稀硫酸中加入适量氧化铜粉末
【答案】D
【解析】
A、向一定量的硫酸铜溶液中加入足量镁粉,则置换出来的铜的质量大于参加反应的镁的质量,溶液的质量会减小,错误;B、向饱和的硝酸钾溶液中加入足量硝酸钾,硝酸钾不再溶解,溶液质量不变,错误;C、向一杯接近饱和的石灰水中加入少量氧化钙,氧化钙与水反应生成氢氧化钙,溶液质量减小,错误;D、向一定量的稀硫酸中加入适量氧化铜粉末,则反应生成硫酸铜,溶液的质量增大,正确。故选D。

 高中必刷题系列答案
高中必刷题系列答案【题目】如图是教材探究二氧化锰对过氧化氢的分解反应是否具有催化作用的实验装置图。请回答下列问题。
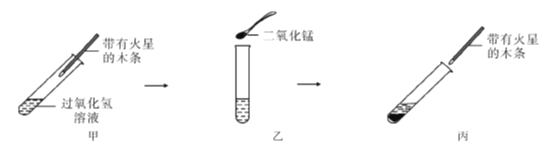
(1)丙图的实验现象是____________________,根据甲图实验的现象和丙图实验的现象的对比,可以说明二氧化锰对过氧化氢反应的影响是________________;此过程发生反应的化学方程式为_____________。
(2)如果在实验前用精密天平称量二氧化锰的质量,实验后把二氧化锰______________(填“操作”),再称量,发现二氧化锰的质量没有改变。
(3)仅凭上述实验还不能说明二氧化锰是过氧化氢分解反应的催化剂,因为上述实验还没有探究二氧化锰的化学性质是否改变,具体的做法是___________________________________________________。
(4)下表是张南同学探究影响H2O2分解因素时所记录的部分数据,通过对数据分析,你能得出的结论是______。
用足量等体积H2O2溶液制取相同体积O2所需的时间
催化剂/时间(min)/浓度 | 30%H2O2溶液 | 15%H2O2溶液 | 5%H2O2溶液 |
加入Wg MnO2 | 0.2 | 0.8 | 2.0 |
【题目】某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验。
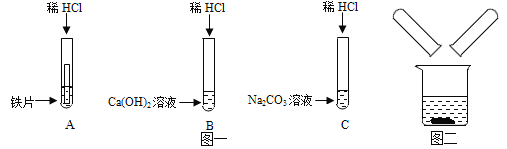
(1)写出实验A中的反应现象_____。
(2)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个清净的烧杯中(如图二所示)观察到先有气泡产生,后有白色沉淀生成。同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究。
写出上述生成白色沉淀的化学反应方程式_____。
(提出猜想)
甲同学猜想:NaCl;
乙同学猜想:NaCl、CaCl2;
丙同学猜想:NaCl、CaCl2、HCl;
你的猜想:_____。
(交流讨论)你认为_____同学的猜想一定不正确,理由是_____。
(设计实验)请设计实验证明你的猜想正确。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,向其中滴加_____ | _____ | 猜想成立 |
【题目】氧气是我们身边无法离开的物质。某兴趣小组对氧气的研究如下:
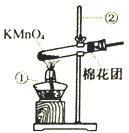
I.氧气的制备:
(1)写出上图中有标号仪器的名称:①___________,②__________。
(2)写出用KMnO4制取O2的化学反应方程式__________________。该装置中棉花团的作用是_______,图中装置一处明显的错误是______________。
II.氧气的收集:
[实验1]用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃时停止收集,测定瓶中氧气的含量,重复实验3次。
[实验2]用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃后,继续收集40秒,测定瓶中氧气的含量,重复实验3次。
[实验3]用排水法收集氧气,测定瓶中氧气的含量,重复实验3次。
实验数据:
实验1 | 实验2 | 实验3 | ||||||||
氧气的体积分数(%) | 79.7 | 79.6 | 79.9 | 88.4 | 89.0 | 87.9 | 90.0 | 89.8 | 89.3 | |
氧气的平均体积分数(%) | 79.7 | 88.4 | 89.7 | |||||||
数据
(3)由实验1、2可知,用向上排空气法收集氧气时,为提高获得的氧气体积分数,可采取的措施是_________。
(4)不考虑操作因素,实验3获得的氧气体积分数不能达到100%的主要原因是_______。
Ⅲ.铁丝在氧气中燃烧
(5)铁丝在纯净氧气中燃烧的化学反应方程式为________________________。
(6)铁丝燃烧时火星四射,经研究表明产生火星四射现象的原因,可能是同时生成了某种气体,推测该气体是_____________(填化学反应文字表达式)。