题目内容
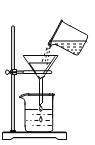
【题目】用氢氧化钠溶液和稀盐酸进行中和反应实验,具体操作如图所示。

在烧杯中加入10mL的氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液呈__色。接着加入一定量的稀盐酸,用玻璃棒搅拌后发现溶液为无色,此时__(填“能”或“不能”)得出两者恰好中和的结论。以下操作及实验现象能证明加入的盐酸为过量的是______(填字母序号)。
A 加入少量铁粉,无明显现象
B 滴加紫色石蕊溶液,搅拌后溶液变蓝
C 加入碳酸钠溶液,产生气泡
【答案】红 不能 C
【解析】
碱性溶液能使无色酚酞试液变红色。在烧杯中加入10mL的氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液呈红色;接着加入一定量的稀盐酸,用玻璃棒搅拌后发现溶液为无色,此时不能得出两者恰好中和的结论,因为无色酚酞试液在酸性和中性溶液中都不变色;
A、铁能和盐酸反应生成氢气,无明显现象,说明盐酸不过量,不符合题意;
B、酸能使紫色石蕊试液变红色,溶液变蓝,说明加入的盐酸量不足,不符合题意;
C、碳酸钠能和盐酸反应生成二氧化碳气体,有气泡产生,说明盐酸过量,符合题意。故选C。

【题目】小晨同学从课外读物中得知:在加热条件下,钠与CO2反应的产物可能有C、CO、Na2CO3、Na2O。于是设计实验对产物成分进行探究。
(查阅资料)①BaCl2溶液呈中性;②4Na+O2=2Na2O;③Na2O+H2O=2NaOH;④2Na+2H2O=2NaOH+H2↑;⑤CO通入PdCl2溶液中有黑色沉淀生成。
(提出问题)在加热条件下,钠与CO2反应的产物有哪些?
(猜想假设)猜想一:产物中一定有C 猜想二:产物中一定有CO
猜想三:产物中一定有Na2CO3 猜想四:产物中一定有Na2O
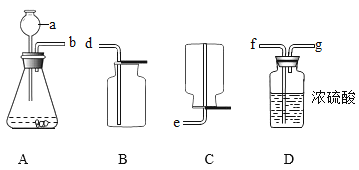
(实验验证)用下图所示装置(夹持装置已略去)进行实验探究。
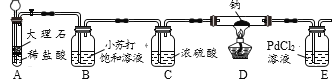
装置A中发生反应的化学方程式为_____;装置C的作用是_____。
序号 | 实验操作 | 实验现象 | 实验结论 |
(1) | 待钠完全反应后,将装置D中的固体置于烧杯中,加蒸馏水溶解 | 有黑色不溶物 | 猜想____正确 |
(2) | 将实验(1)所得混合物过滤,取滤液加入过量BaCl2溶液 | _____ | 猜想三正确 |
(3) | _____ | 猜想二正确 |
(反思与评价)小晨同学向实验(2)所得溶液中滴入几滴酚酞溶液,溶液呈红色。 于是得出结论:在加热条件下,钠与CO2反应一定产生Na2O。该结论是否严谨?____(填“是”或“否”),理由是____。