题目内容
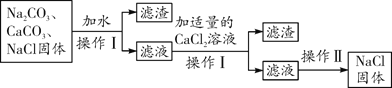
【题目】现有一包混有少量Na2CO3和CaCO3的NaCl固体,为除去其中的杂质,设计流程如图,请回答下列问题:
(1)在操作Ⅰ前加入水的目的____________。
(2)操作II名称是__________,其中玻璃棒的作用是__________
(3)写出除杂过程中发生的化学方程式__________。该反应属于____________(填写基本反应类型)。
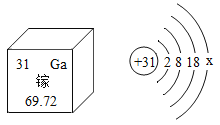
(4)求出Na2CO3中碳元素的化合价:______________。
【答案】将固体物质溶解,分离碳酸钙 蒸发 搅拌加快蒸发的速率,防止局部过热 Na2CO3+CaCl2=2NaCl+CaCO3↓ 复分解反应 ![]()
【解析】
碳酸钙、碳酸钠、氯化钠混合固体加水溶解,过滤得到滤渣成分为碳酸钙(不溶解),滤液为碳酸钠和氯化钠混合溶液,加入适量的氯化钙与碳酸钠恰好完全反应:Na2CO3+CaCl2=2NaCl+CaCO3↓,此时溶液中只有碳酸钠,再次过滤掉碳酸钙,最后浓缩蒸发溶剂,得到氯化钠固体。
(1)由于碳酸钙不能溶于水,在操作Ⅰ前加入水的目的:将固体物质溶解,分离碳酸钙;
(2)操作II是将氯化钠溶液中蒸发得到氯化钠,实验操作为:蒸发,其中玻璃棒在蒸发操作中的作用是:蒸发,搅拌加快蒸发的速率,防止由于局部温度过热造成液体飞溅;
(3)除杂过程中加入氯化钙除去碳酸钠的反应原理是:Na2CO3+CaCl2=2NaCl+CaCO3↓该反应属于复分解反应;
(4)求出Na2CO3中碳元素的化合价,设:碳元素化合价为x,(+1)×2+x+(-2)×3=0,则
x=+4;故Na2CO3中碳元素的化合价:![]() 。
。

 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
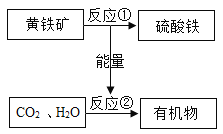
轻松课堂单元测试AB卷系列答案【题目】化学兴趣小组的同学获得两包制作“跳跳糖”的添加剂,一包是柠檬酸晶体,另一包是标注为钠盐的白色粉末。同学们将少量柠檬酸和这种白色粉未溶于水,混合后产生了使澄清石灰水变浑浊的气体,于是他们对白色粉末的化学成分进行了以下探究:
(提出猜想)猜想1.碳酸钠;猜想2.碳酸氢钠;猜想3.___________。
(查阅资料)①碳酸钠溶液、碳酸氢钠溶液均呈碱性;② 碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;碳酸钠受热不分解
(实验探究)兴趣小组设计不同实验方案进行探究。
甲组方案:将白色粉末溶于水后用pH试纸测定其酸碱度,pH>7猜想1正确
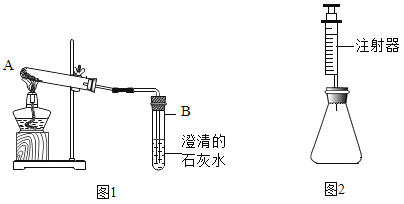
乙组方案:如图1,取适量白色粉末于试管中,将导管伸入澄清石灰水,加热,澄清石灰水变浑浊,猜想2正确,写出装置B中反应的化学方程式______________。
丙组方案:用如图2所示装置作为反应容器,准确测量生成气体的体积以判断白色粉末的成分。分别向盛有碳酸钠、碳酸氢钠和白色粉末的锥形瓶中,注入等体积、等浓度的足量的稀盐酸,记录如表:
实验编号 | 锥形瓶内物质[来源 | 最终得到 CO2 体积/mL | |
名称 | 质量/g | ||
① | 碳酸钠 | a | V1 |
② | 碳酸氢钠 | a | V2 |
③ | 白色粉末 | m | V3 |
实验①的化学反应方程式为____________; 表中 m=_______g; 根据上表中数据分析,猜想3正确,判断的依据是__________。
(交流反思)大家讨论后认为甲、乙组的结论都不准确:不准确的原因,甲是__________;乙是_____________。
(结论分析)探究后他们核查到添加剂的成分是柠檬酸和碳酸氢钠,分析后认为白色粉末中的碳酸钠是由碳酸氢钠分解产生的。
(拓展应用)下列物质常温下放置一段时间也会分解的是________(填序号)。
A 碳酸 B 氨水 C 碳酸氢铵 D 盐酸