题目内容
【题目】已知氢气可以在氯气中燃烧,其反应的化学方程式为:![]() 。在一密闭容器中盛有H2、O2、Cl2的混合气体,已知其分子数之比为11∶5∶1,用电火花点燃,使其充分反应,冷却后所得溶液的质量分数为( )
。在一密闭容器中盛有H2、O2、Cl2的混合气体,已知其分子数之比为11∶5∶1,用电火花点燃,使其充分反应,冷却后所得溶液的质量分数为( )
A.40.3%
B.28.9%
C.44.8%
D.30.5%
【答案】B
【解析】
在一密闭容器中盛有H2、O2、Cl2的混合气体,已知其分子数之比为11∶5∶1,用电火花点燃,会发生两个反应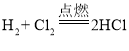 和
和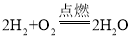 。
。
根据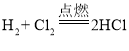 ,反应的氢气分子、氯气分子和氯化氢分子的分子个数比为1:1:2,
,反应的氢气分子、氯气分子和氯化氢分子的分子个数比为1:1:2,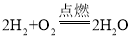 反应中,反应的氢气分子、氧气分子和水分子的分子个数比为2:1:2=10:5:10,所以密闭容器中参加反应的氢气分子、氧气分子与氯气分子的个数比为11:5:1,恰好完全反应,生成氯化氢和水的分子个数比为2:10=1:5,故生成氯化氢和水的质量比为:36.5:(18×5)=36.5:90,又因为生成的氯化氢气体极易溶于水,所以会形成盐酸溶液,所得溶液的质量分数为
反应中,反应的氢气分子、氧气分子和水分子的分子个数比为2:1:2=10:5:10,所以密闭容器中参加反应的氢气分子、氧气分子与氯气分子的个数比为11:5:1,恰好完全反应,生成氯化氢和水的分子个数比为2:10=1:5,故生成氯化氢和水的质量比为:36.5:(18×5)=36.5:90,又因为生成的氯化氢气体极易溶于水,所以会形成盐酸溶液,所得溶液的质量分数为![]() 。故选B。
。故选B。

练习册系列答案
相关题目