��Ŀ����
����Ŀ��ij��ȤС��ͬѧ��ʵ�����Ʊ�������������������̽��ʵ�顣
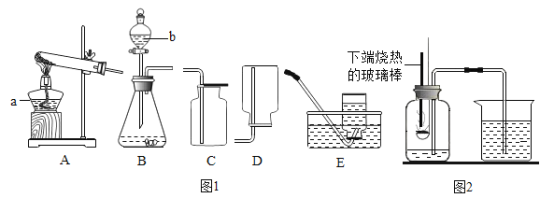
��1��Ϊ̽����������
�������طֽ��ٶȵ�Ӱ�죬��������¶Ա�ʵ�飺
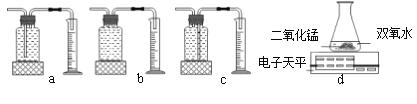
��.��3.0g �������1.0g �������̣�MnO2�����Ȼ�ϼ���
��xg�������1.0g����ͭ ��CuO�����Ȼ�ϼ�������ͬ�¶��£��Ƚ�����ʵ�����O2�Ŀ�����
���з�Ӧ�����ֱ���ʽ��_________________������x��ֵӦΪ______��
��2����̽����Ӱ��˫��ˮ�ֽ��ٶȵ�ij�����ء�ʵ�����ݼ�¼���£�
˫��ˮ������ | ˫��ˮ��Ũ�� | MnO2������ | ��ͬʱ���ڲ���O2��� | |
�� | 50.0g | 1% | 0.1g | 9mL |
�� | 50.0g | 2% | 0.1g | 16mL |
�� | 50.0g | 4% | 0.1g | 31mL |
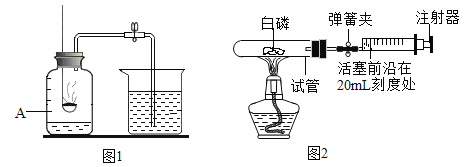
��ʵ���У�����O2�����װ����______�����ţ���
ʵ����ۣ�����ͬ�����£�_______________��˫��ˮ�ֽ��Խ�졣������ͼdװ�ý���ʵ�飬ͨ���Ƚ�___________________Ҳ�ܴﵽʵ��Ŀ�ġ�
���𰸡������ �Ȼ���+������3.0��c��˫��ˮŨ��Խ����ͬʱ����ƽ������ֵ��С
�Ȼ���+������3.0��c��˫��ˮŨ��Խ����ͬʱ����ƽ������ֵ��С
��������
��1�����ݿ�������ص������Ͷ������̺�����ͭ��������Ȳ��ܱȽϳ��������̺�����ͭ�Ĵ�Ч��������
��2����������̹ܽ����ܳ������ų��Լ�ƿ�е�ˮ������ʵ�����ݺ���ͬʱ���ڲ���O2����������������ݳ����ڳ��ڵ�������ʣ�����ʵ�����������з�����
��1��������ڶ��������������������·ֽ���Ȼ��غ���������Ӧ�����ֱ���ʽ�������![]() �Ȼ���+���������ƿ�������ص������Ͷ������̺�����ͭ��������Ȳ��ܱȽϳ��������̺�����ͭ�Ĵ�Ч��������x��ֵӦΪ3.0g��
�Ȼ���+���������ƿ�������ص������Ͷ������̺�����ͭ��������Ȳ��ܱȽϳ��������̺�����ͭ�Ĵ�Ч��������x��ֵӦΪ3.0g��
��2������̹ܽ����ܳ������ų��Լ�ƿ�е�ˮ����ѡC��
ʵ����ۣ��ӱ���ʵ�����ݿ�֪����ͬ�����£�˫��ˮ��Ũ��Խ��������������Խ�죻
������ͼ��dװ�ý���ʵ�飬���������ݳ������ڵ�������ʣ�����ʵ��������ᣬ����������������ɵ�����������������ͨ���Ƚ���ͬʱ����ƽ������ֵ��СҲ�ܴﵽʵ��Ŀ����

 ˫��ͬ������ѵ��ϵ�д�
˫��ͬ������ѵ��ϵ�д� �Ƹ�С״Ԫͬ������������ϵ�д�
�Ƹ�С״Ԫͬ������������ϵ�д�