题目内容
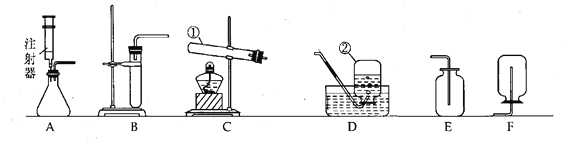
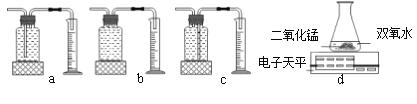
【题目】如图1是化学实验室几种常用的实验装置图,请回答:
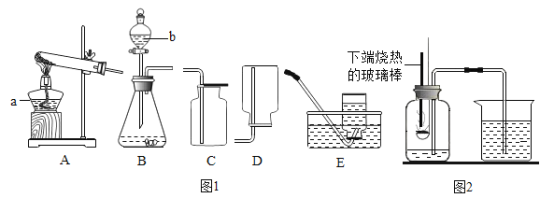
(1)写出仪器a、b的名称:a是____________;b是__________。
(2)某同学用(高锰酸钾)A装置制取氧气, 该装置需改进的一处是___________,
写出该反应的文字表达式:_______________________________________;
用A装置制氧气另一反应的文字表达式:__________________________。
(3)若用B装置制取氧气时,锥形瓶中放入的物质名称是________,b仪器中加入的物
质名称是________,写出该反应的符号表达式:_____________________。
(4)甲烷是密度小于空气、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,制取甲烷的发生装置应选择______(填装置编号,下同),收集装置应选__________。
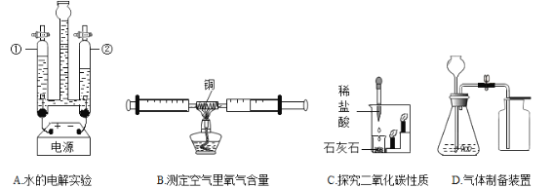
(5)如图2是“空气中氧气体积分数测定”实验的改进装置。
主要操作是:在实际容积为130mL的集气瓶里,先装进30mL的水,再按图连好仪器,按下热的玻璃棒,白磷立即被点燃。
①白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是__________________;
若实验非常成功,最终集气瓶中水的体积约为__________ml。
②集气瓶里预先装进的30mL水,在实验过程中起到哪些作用?_________(填写序号)
a.加快集气瓶冷却 b.液封导气管末端以防气体逸出
c.缓冲集气瓶内气压的骤然升高
【答案】酒精灯分液漏斗试管口应放一团棉花高锰酸钾![]() 锰酸钾+二氧化锰+氧气氯酸钾
锰酸钾+二氧化锰+氧气氯酸钾![]() 氯化钾+氧气二氧化锰过氧化氢或双氧水H2O2
氯化钾+氧气二氧化锰过氧化氢或双氧水H2O2![]() H2O+O2AD或E水面先下降后上升50mlabc
H2O+O2AD或E水面先下降后上升50mlabc
【解析】
(1)图中标号仪器的名称:a是酒精灯;b是分液漏斗;
(2)实验室用高锰酸钾制取氧气时,试管口需要放一团棉花,防止高锰酸钾粉末进入导管,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的文字表达式为:高锰酸钾![]() 锰酸钾+二氧化锰+氧气;实验室还常用加热氯酸钾制氧气,氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,该反应的文字表达式为:氯酸钾
锰酸钾+二氧化锰+氧气;实验室还常用加热氯酸钾制氧气,氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,该反应的文字表达式为:氯酸钾![]() 氯化钾+氧气;
氯化钾+氧气;
(3)采用B装置制取氧气时,锥形瓶中放入的物质名称是二氧化锰,分液漏斗中加入的物质是过氧化氢溶液;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气;该反应的符号表达式为:H2O2![]() H2O+O2;
H2O+O2;
(4)实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,属于固体加热型,应该选用的发生装置是A;甲烷密度小于空气、难溶于水,可选用能用向下排空气法、排水法收集,即收集装置是D或E;
(5)①白磷从燃烧到熄灭冷却的过程中,瓶内的压强先增大,后又降低,因此瓶内水面的变化是先下降,后上升;由于空气中氧气约占空气体积的五分之一,容积为130mL的集气瓶里,先装进30mL的水,所以空气体积是100mL,所以氧气占20mL,所以最后集气瓶中水的体积约为30mL+20mL=50mL;
②集气瓶内预先装入适量的水,使白磷燃烧时集气瓶内气压不会过度增大,不至于使集气瓶中气体受热膨胀而逸出;同时还可以加快集气瓶冷却,缓冲集气瓶内气压的骤然升高。

 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
(1)为探究催化剂的种
类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g 氯酸钾与1.0g 二氧化锰(MnO2)均匀混合加热
Ⅱ.将xg氯酸钾与1.0g氧化铜 (CuO)均匀混合加热在相同温度下,比较两组实验产生O2的快慢。
Ⅰ中反应的文字表达式是_________________。Ⅱ中x的值应为______。
(2)乙探究了影响双氧水分解速度的某种因素。实验数据记录如下:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9mL |
Ⅱ | 50.0g | 2% | 0.1g | 16mL |
Ⅲ | 50.0g | 4% | 0.1g | 31mL |
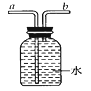
本实验中,测量O2体积的装置是______(填编号)。
实验结论:在相同条件下,_______________,双氧水分解得越快。丙用下图d装置进行实验,通过比较___________________也能达到实验目的。