题目内容
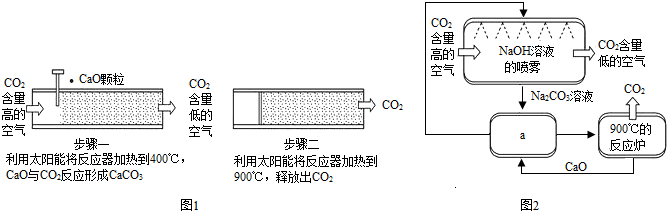
空气中CO2浓度的持续走高引起人们的高度重视.一些科学家认为,人类不仅要努力减少CO2的排放,还要尽快想办法清除空气中过多的CO2.为此,他们设想了一系列“捕捉”和“封存”CO2的方法.图是一些科学家利用NaOH溶液的喷淋“捕捉”空气中的CO2,并利用CO2生产甲醇(CH3OH)的一种方法.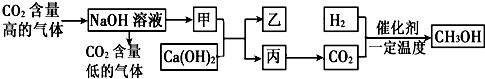
①过多的CO2排放到空气中会引起
②NaOH溶液喷成雾状是为了
③为了尽量减少成本,在整个流程中,循环利用的物质有Ca(OH)2和
④往饱和NaOH溶液中通入过量的CO2,析出碳酸氢钠晶体,该反应化学方程式:
⑤.下列溶液中,同样能用于“捕捉”二氧化碳的是
A.KNO3溶液 B.CaCl2溶液 C.CuSO4溶液 D.Na2CO3溶液.

①过多的CO2排放到空气中会引起
温室效应
温室效应
.“尿素生产技术”可使“捕捉”的CO2转化成尿素,尿素属于农业广泛使用的化学肥料中的氮肥
氮肥
.②NaOH溶液喷成雾状是为了
增大反应物接触面积(提高吸收效率)
增大反应物接触面积(提高吸收效率)
.写出NaOH溶液“捕捉”CO2 的化学方程式:CO2+2NaOH═Na2CO3+H2O
CO2+2NaOH═Na2CO3+H2O
③为了尽量减少成本,在整个流程中,循环利用的物质有Ca(OH)2和
NaOH或CaO
NaOH或CaO
.④往饱和NaOH溶液中通入过量的CO2,析出碳酸氢钠晶体,该反应化学方程式:
NaOH+CO2═NaHCO3
NaOH+CO2═NaHCO3
⑤.下列溶液中,同样能用于“捕捉”二氧化碳的是
D
D
.A.KNO3溶液 B.CaCl2溶液 C.CuSO4溶液 D.Na2CO3溶液.
分析:①根据造成温室效应的气体考虑;②根据化学肥料的分类方法考虑;③循环利用必须是既作为反应物,又会在生成物中出现;④根据方程式的书写方法考虑;⑤能用于“捕捉”二氧化碳的物质必须能与二氧化碳反应将其吸收.
解答:解:①造成的温室效应的气体有:二氧化碳、甲烷、臭氧等,主要气体是二氧化碳,所以过多的CO2排放到空气中会引起温室效应;化肥中含有氮元素的属于氮肥,含有磷元素的是磷肥,含钾元素的属于钾肥,含有氮、磷、钾三种元素中的两种或三种属于复合肥,所以尿素属于氮肥;
②NaOH溶液喷成雾状能增加氢氧化钠与二氧化碳的接触面积,提高了氢氧化钠溶液对二氧化碳的吸收率;NaOH溶液“捕捉”CO2 的反应物是氢氧化钠和二氧化碳,生成物是碳酸钠和水,用观察法配平即可;
③循环利用必须是既作为反应物,又会在生成物中出现,碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,氢氧化钠还可以吸收二氧化碳,碳酸钙高温生成氧化钙和二氧化碳,氧化钙与水反应生成氢氧化钙,氢氧化钙可与碳酸钠反应,所以氢氧化钠与氧化钙可循环使用;
④往饱和NaOH溶液中通入过量的CO2,析出碳酸氢钠晶体的反应物是氢氧化钠和二氧化碳,生成物是碳酸氢钠;
⑤能用于“捕捉”二氧化碳的物质必须能与二氧化碳反应,才能能吸收二氧化碳,KNO3溶液、CaCl2溶液、CuSO4溶液 都不能与二氧化碳反应,碳酸钠溶液可以与二氧化碳反应,能吸收二氧化碳.
②NaOH溶液喷成雾状能增加氢氧化钠与二氧化碳的接触面积,提高了氢氧化钠溶液对二氧化碳的吸收率;NaOH溶液“捕捉”CO2 的反应物是氢氧化钠和二氧化碳,生成物是碳酸钠和水,用观察法配平即可;
③循环利用必须是既作为反应物,又会在生成物中出现,碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,氢氧化钠还可以吸收二氧化碳,碳酸钙高温生成氧化钙和二氧化碳,氧化钙与水反应生成氢氧化钙,氢氧化钙可与碳酸钠反应,所以氢氧化钠与氧化钙可循环使用;
④往饱和NaOH溶液中通入过量的CO2,析出碳酸氢钠晶体的反应物是氢氧化钠和二氧化碳,生成物是碳酸氢钠;
⑤能用于“捕捉”二氧化碳的物质必须能与二氧化碳反应,才能能吸收二氧化碳,KNO3溶液、CaCl2溶液、CuSO4溶液 都不能与二氧化碳反应,碳酸钠溶液可以与二氧化碳反应,能吸收二氧化碳.
点评:解答本题关键是要熟悉温室效应的气体,知道方程式的书写方法,知道能循环利用的物质,必须既能作为反应物,又在生成物中出现.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目