题目内容
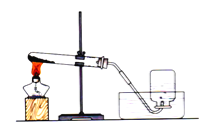
【题目】经过一月的学习,你已经初步掌握实验室制取气体的有关知识,请结合图示回答问题:

(1)写出图中标号仪器的名称:① ;② 。
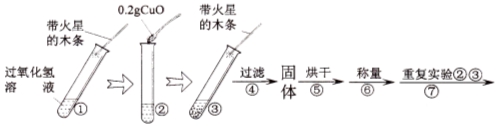
(2)实验室用氯酸钾制取氧气,应选用的发生装置是 ,(填字母序号,下同),该反应的化学表达式为 ,若要收集一瓶干燥的氧气,应选择的收集装置是 。
(3)实验室用H2O2溶液和MnO2混合制氧气,其中MnO2起 作用,应选择的发生和收集装置是 。同学们利用B和F装置,通过排水量来测定生成氧气的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏大(水的体积测量准确),其主要原因是 。
(4)实验室制取CO2发生装置可选用 ,收集CO2通常选用装置 _ (填写装置序号);判断CO2已收集满的方法是 ;
(5)用高锰酸钾制取O2,装置A还需做的一点改动是 ;发生反应的化学表达式为 ;
(6)若用如图所示H塑料袋排空气法收集H2,则H2导入端为 (填“a”或“b”)

(7)用如图I所示的矿泉水瓶进行对比实验时,可以证明CO2与澄清石灰水确实发生了反应,应作的对比实验是 。

(8)实验室常用如图装置代替装置B制取气体,该装置的优点是 ,下列反应适用于该装置的是 (填序号)。
①大理石和稀盐酸 ②碳酸钠粉末和稀硫酸
③锌粒与稀硫酸 ④过氧化氢溶液与二氧化锰
(9)B装置的优点是 ;其中的分液漏斗可用 。
【答案】(1)、酒精灯、锥形瓶:(2)、A、氯酸钾![]() 氯化钾+氧气、E:(3)、催化、BC/BF,包含了滴入液体的体积;(4)、B、E、将燃着的木条平放于瓶口,若熄灭,则收集满;(5)、管口处放一团棉花;高锰酸钾
氯化钾+氧气、E:(3)、催化、BC/BF,包含了滴入液体的体积;(4)、B、E、将燃着的木条平放于瓶口,若熄灭,则收集满;(5)、管口处放一团棉花;高锰酸钾![]() 锰酸钾+二氧化锰+氧气;(6)、b;(7)、把石灰水换作等体积的水;(8)、控制反应的发生与停止;①③;(9)、通过控制液体的滴加量达到控制反应速率的目的;注射器;
锰酸钾+二氧化锰+氧气;(6)、b;(7)、把石灰水换作等体积的水;(8)、控制反应的发生与停止;①③;(9)、通过控制液体的滴加量达到控制反应速率的目的;注射器;
【解析】
试题分析:(1)图中标号仪器的名称:①酒精灯;②锥形瓶;(2)实验室用氯酸钾制取氧气,因为是固体加热制取气体,故应选用的发生装置是A,该反应的化学表达式为氯酸钾![]() 氯化钾+氧气,若要收集一瓶干燥的氧气,应选择的收集装置是向上排空气法E。(3)实验室用H2O2溶液和MnO2混合制氧气,其中MnO2起催化作用,应选择的发生和收集装置是固液常温形装置和排水集气法、向上排空气法收集。同学们利用B和F装置,通过排水量来测定生成氧气的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏大(水的体积测量准确),其主要原因是滴加过氧化氢时,装置内的气体把水压入量筒中;(4)实验室制取CO2因为用大理石和盐酸常温下反应,发生装置可选用B,生成的二氧化碳能溶于水,且密度比空气大,故收集CO2通常选用装置E,(5)用高锰酸钾制取O2,装置A还需在管口处放一团棉花,发生反应的化学表达式为高锰酸钾
氯化钾+氧气,若要收集一瓶干燥的氧气,应选择的收集装置是向上排空气法E。(3)实验室用H2O2溶液和MnO2混合制氧气,其中MnO2起催化作用,应选择的发生和收集装置是固液常温形装置和排水集气法、向上排空气法收集。同学们利用B和F装置,通过排水量来测定生成氧气的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏大(水的体积测量准确),其主要原因是滴加过氧化氢时,装置内的气体把水压入量筒中;(4)实验室制取CO2因为用大理石和盐酸常温下反应,发生装置可选用B,生成的二氧化碳能溶于水,且密度比空气大,故收集CO2通常选用装置E,(5)用高锰酸钾制取O2,装置A还需在管口处放一团棉花,发生反应的化学表达式为高锰酸钾![]() 锰酸钾+二氧化锰+氧气;(6)用右图所示H塑料袋排空气法收集H2,则H2导入端为b进入,因为氢气的密度比空的小,浮在装置的上方,把空气排出;(7)用右图I所示的矿泉水瓶进行对比实验时,可以证明CO2与澄清石灰水确实发生了反应,应作的对比实验是把石灰水换作等体积的水;(8)实验室常用右图装置代替装置B制取气体,该装置的优点是能随时控制反应的发生与停止;反应适用于块状固体和液体常温下反应,故选择①③;(9)B装置的优点是通过控制液体的滴加量达到控制反应速率的目的,其中的分液漏斗可用注射器。
锰酸钾+二氧化锰+氧气;(6)用右图所示H塑料袋排空气法收集H2,则H2导入端为b进入,因为氢气的密度比空的小,浮在装置的上方,把空气排出;(7)用右图I所示的矿泉水瓶进行对比实验时,可以证明CO2与澄清石灰水确实发生了反应,应作的对比实验是把石灰水换作等体积的水;(8)实验室常用右图装置代替装置B制取气体,该装置的优点是能随时控制反应的发生与停止;反应适用于块状固体和液体常温下反应,故选择①③;(9)B装置的优点是通过控制液体的滴加量达到控制反应速率的目的,其中的分液漏斗可用注射器。

【题目】某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰。该小组同学进行了如下探究。
(1)写出铁丝在氧气中燃烧的化学反应文字表达式: 。
(2)探究一:蜡烛燃烧产生火焰的原因是什么?

点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。由此可知:蜡烛燃烧产生的火焰是由 (填“固态”或“气态”)物质燃烧形成的。
(3)探究二:物质燃烧产生火焰的根本原因是什么?
【查阅资料】
物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
石蜡 | 50∽70 | 300∽550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
由该表可知:物质燃烧能否产生火焰与其 (填“熔点”或“沸点”)和燃烧时温度有关。由此推测:钠在燃烧时, (填“有”或“没有”)火焰产生。
(4)木炭在氧气中燃烧没有火焰,但生活中同样的木炭燃烧时会产生火焰,其原因可能是 。