题目内容
李明同学设计了两种以铁、氧化铜、稀硫酸为原料制取金属铜的方法.(已知:H2+CuO═Cu+H2O)
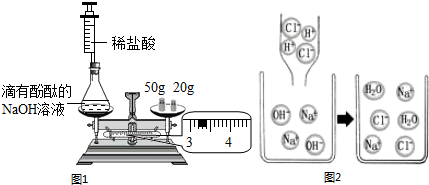
(1)第一种方法的实验过程中有蓝色溶液产生,你认为李明同学应选用下述装置中的(填装置的序号 .

(2)第一种方法的实验过程中,为了缩短反应的时间,必需加快化学反应速率.你认为李明同学采取加快反应速率的措施是: .
(3)写出第一种方法中有关的反应化学方程式 .
(4)用这两种方法制得铜中都可能含有杂质.则第二种方法制得的铜中,可能含有的杂质是: .
(5)若用这两种方法制取铜的质量相等,下列叙述符合实际实验结果的是 .
A、消耗氧化铜的质量相等 B、消耗铁的质量相等
C、消耗硫酸的质量相等 D、生成硫酸亚铁的质量不相等
(6)取用第二种方法制得的铜样品(含杂质)10g,放入50g的稀硫酸中二者恰好完全反应,然后过滤、洗涤、干燥,发现铜样品的质量为8.4g.求稀硫酸中溶质的质量分数.
(1)第一种方法的实验过程中有蓝色溶液产生,你认为李明同学应选用下述装置中的(填装置的序号

(2)第一种方法的实验过程中,为了缩短反应的时间,必需加快化学反应速率.你认为李明同学采取加快反应速率的措施是:
(3)写出第一种方法中有关的反应化学方程式
(4)用这两种方法制得铜中都可能含有杂质.则第二种方法制得的铜中,可能含有的杂质是:
(5)若用这两种方法制取铜的质量相等,下列叙述符合实际实验结果的是
A、消耗氧化铜的质量相等 B、消耗铁的质量相等
C、消耗硫酸的质量相等 D、生成硫酸亚铁的质量不相等
(6)取用第二种方法制得的铜样品(含杂质)10g,放入50g的稀硫酸中二者恰好完全反应,然后过滤、洗涤、干燥,发现铜样品的质量为8.4g.求稀硫酸中溶质的质量分数.
考点:化学实验方案设计与评价,有关溶质质量分数的简单计算,根据化学反应方程式的计算
专题:溶质质量分数与化学方程式相结合的计算,简单实验方案的设计与评价
分析:根据铁、氧化铜、稀硫酸三种物质之间的反应规律分析解答,氧化铜能与稀硫酸反应生成硫酸铜,铁能置换硫酸铜溶液中的铜;铁能与稀硫酸反应生成氢气,氢气能置换氧化铜中的铜.利用两种途径的过程,书写相应的化学方程式,根据反应的物质之间量的关系进行判断,从氢气还原氧化铜,氢气必须过量,所以要使用更多锌更多硫酸,制取相同质量的铜,铜只来源于氧化铜,所以消耗的氧化铜质量相等,利用这些关系解决此题.
解答:解:(1)用铁、氧化铜、稀硫酸三种物质制取铜,实验过程中有蓝色溶液产生,因此方法是将氧化铜与硫酸反应生成硫酸铜,然后将铁与硫酸铜反应置换出铜,采用过滤法即可得到铜.故选用的装置应为CE;故填:CE;
(2)加热可以加快氧化铜和硫酸反应速率,所以可以采取加热反应物的方法来加快反应速率;故填:加热反应物;
(3)氧化铜和硫酸反应生成硫酸铜和水,硫酸铜溶液和铁反应生成硫酸亚铁和铜,反应化学方程式分别为:CuO+H2SO4=CuSO4+H2O,CuSO4+Fe=Cu+FeSO4 ;故填:CuO+H2SO4=CuSO4+H2O,CuSO4+Fe=Cu+FeSO4 ;
(4)第二种方法是铁与稀硫酸反应生成氢气,氢气置换氧化铜中的铜,如果氢气的量不足,就会有氧化铜剩余,所以可能含有的杂质是氧化铜;故填:氧化铜;
(5)因为整个制备过程中,所有Cu元素都能形成单质Cu,而都来自CuO,没有损失,所以①②氧化铜质量相同.
①Fe+H2SO4=FeSO4+H2↑,H2+CuO
H2O+Cu 生成1份Cu需要1份CuO和1份H2SO4和1份Fe
②CuO+H2SO4=CuSO4+H2O,CuSO4+Fe=Cu+FeSO4 生成1份Cu需要1份CuO和1份H2SO4和1份Fe
看上去都是相同的.特别注意用H2还原氧化铜的时候,需要先通H2然后加热,以将空气从玻璃管中排出.如果不排出,会引起爆炸,所以H2的量要多一些.自然H2SO4和铁的量也要多一些,同时生成的硫酸亚铁质量可能不同.故选A、D.
(6)设50g的稀硫酸溶液中含硫酸的质量为X,则与硫酸反应的氧化铜的质量为:
10g-8.4g=1.6g
CuO+H2SO4═CuSO4+H2O
80 98g X
=
X=1.96g
所以稀硫酸中溶质的质量分数=
×100%=3.92%
答:稀硫酸中溶质的质量分数为3.92%.
(2)加热可以加快氧化铜和硫酸反应速率,所以可以采取加热反应物的方法来加快反应速率;故填:加热反应物;
(3)氧化铜和硫酸反应生成硫酸铜和水,硫酸铜溶液和铁反应生成硫酸亚铁和铜,反应化学方程式分别为:CuO+H2SO4=CuSO4+H2O,CuSO4+Fe=Cu+FeSO4 ;故填:CuO+H2SO4=CuSO4+H2O,CuSO4+Fe=Cu+FeSO4 ;
(4)第二种方法是铁与稀硫酸反应生成氢气,氢气置换氧化铜中的铜,如果氢气的量不足,就会有氧化铜剩余,所以可能含有的杂质是氧化铜;故填:氧化铜;
(5)因为整个制备过程中,所有Cu元素都能形成单质Cu,而都来自CuO,没有损失,所以①②氧化铜质量相同.
①Fe+H2SO4=FeSO4+H2↑,H2+CuO
| ||
②CuO+H2SO4=CuSO4+H2O,CuSO4+Fe=Cu+FeSO4 生成1份Cu需要1份CuO和1份H2SO4和1份Fe
看上去都是相同的.特别注意用H2还原氧化铜的时候,需要先通H2然后加热,以将空气从玻璃管中排出.如果不排出,会引起爆炸,所以H2的量要多一些.自然H2SO4和铁的量也要多一些,同时生成的硫酸亚铁质量可能不同.故选A、D.
(6)设50g的稀硫酸溶液中含硫酸的质量为X,则与硫酸反应的氧化铜的质量为:
10g-8.4g=1.6g
CuO+H2SO4═CuSO4+H2O
80 98g X
| 80 |
| 98 |
| 1.6g |
| x |
X=1.96g
所以稀硫酸中溶质的质量分数=
| 1.96g |
| 50g |
答:稀硫酸中溶质的质量分数为3.92%.
点评:本题考查考查较为综合,涉及物质的制备和实验设计等问题,侧重于考查学生综合运用化学知识的能力,为高考常见题型,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质的用途主要利用其化学性质的是( )
| A、石墨棒做干电池电极 |
| B、氧气供给呼吸 |
| C、厨房用的铝锅 |
| D、铜用于制造导线 |
物质的性质决定物质的用途.下列说法中,不合理的是( )
| A、氢气可用于作高能燃料 |
| B、灯泡里充稀有气体可以延长使用寿命 |
| C、氮气用作食品包装袋内的填充气以防腐 |
| D、氧气的化学性质非常活泼,能与所有物质发生化学反应 |
下列物质中含有氧分子的是( )
| A、液态空气 | B、高锰酸钾固体 |
| C、蒸馏水 | D、二氧化碳 |

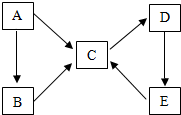 A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如图所示.
A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如图所示.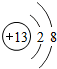 如图为某粒子的结构示意图,下列说法中错误的是
如图为某粒子的结构示意图,下列说法中错误的是