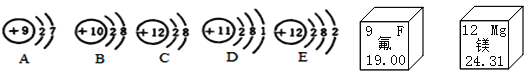题目内容
【题目】(1)用适当的化学符号和数字回答:
①3个磷原子_____;
②保持氧气化学性质最小微粒_____;
③氧化铝中铝元素化合价_____;
④人体血红素中亚铁离子_____ ;
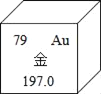
⑤温度计中常用的金属_____;
⑥常用作导线的金属_____。
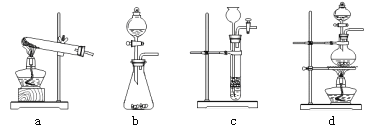
(2)某同学写了以下化学方程式:
A 
B 
C ![]()
D 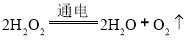
E 
根据化学方程式错误的不同,将其序号填入以下相应的空白处:
①未配平的是_____;
②化学式写错的是_____;
③反应条件写错的是_____;
④未注明反应条件的是_____;
⑤“↑”使用不当的是_____。
【答案】3P O2 ![]() Fe2+ Hg Cu E A D C B
Fe2+ Hg Cu E A D C B
【解析】
(1)①3个磷原子表示为3P。
②氧气是由氧分子构成的,故保持氧气化学性质最小微粒氧分子,化学式为O2。
③氧化铝中铝元素化合价为+3价,表示为![]() 。
。
④人体血红素中亚铁离子表示为Fe2+。
⑤温度计中常用的金属是汞,化学式为Hg。
⑥常用作导线的金属是铜,化学式为Cu。
(2)A、氧化镁化学式书写错误,正确为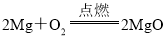 ;
;
B、反应物不打气标符号,正确为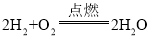 ;
;
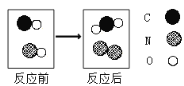
C、铁在氧气中点燃生成四氧化三铁,正确为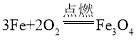 ;
;
D、过氧化氢分解成水和氧气,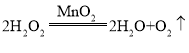 ;
;
E、化学方程式配平错误,正确为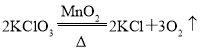 。
。
①未配平的是E;
②化学式写错的是A;
③反应条件写错的是D;
④未注明反应条件的是C;
⑤“↑”使用不当的是B。

【题目】蚊虫叮咬时,会分泌蚁酸.化学小组同学对蚁酸产生了浓厚的兴趣,决定对其进行探究.
[提出问题]蚁酸的成分是什么?它有什么性质?
[查阅资料]I蚁酸的化学名称叫甲酸,化学式为HCOOH
II蚁酸隔绝空气并加热时会分解生成两种氧化物
Ⅲ浓硫酸具有吸水性
[实验探究](1)向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到溶液颜色变成_____色,说明蚁酸显酸性.
(2)小芳同学根据蚁酸中含有______元素,推测出蚁酸在隔绝空气并加热分解时生成水.
(3)对它分解生成的另一种氧化物,小敏提出两种猜想:猜想Ⅰ是CO2; 猜想Ⅱ是____________;
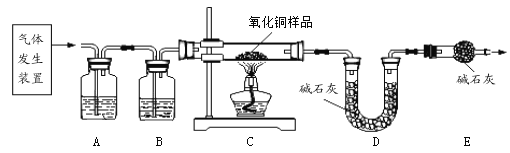
他们按如图所示进行实验:先向装置中通入一会N2,再将蚁酸分解产生的气体通入其中.
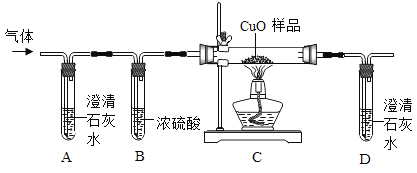
①先通N2的目的是_________________;
②若装置A中无明显变化,则猜想Ⅰ________(填“成立”或“不成立”);
③装置C发生反应的方程式为_______________________;
④装置D中的现象为_________________________;
[结论]甲酸受热能分解,反应的化学方程式是____________________;
[讨论交流]从环保角度看,该装置存在的明显缺陷是_________________.
[拓展延伸]小组同学利用蚁酸分解产生的气体,测定C装置中10g氧化铜样品(杂质不参与反应)中氧化铜的质量分数,在不同时刻测定C中固体的质量(如表):
反应时间/min | 2 | 4 | 6 | 8 | 10 |
固体质量/g | 9.3 | 8.8 | 8.5 | 8.4 | 8.4 |
分析表中数据,完成以下问题:
①在称量质量过程中,必须把玻璃管两端封住,目的是_________________;
②样品中氧化铜的质量分数是________________?
【题目】取10g石灰石样品于烧杯中,再向其中加入足量稀盐酸(杂质不反应),有关实验数据见下表:
反应前 | 反应后 | |
烧杯与稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
160g | 10g | 166.7g |
(1)CaCO3中Ca元素的质量分数为____________。
(2)生成CO2的质量____________。
(3)求石灰石样品中碳酸钙的质量分数____________(写出计算过程)。