题目内容
长久使用的热水瓶底部有一层水垢,主要成分是CaCO3和Mg(OH)2,某学校化学研究小组的同学通过实验测定水垢中CaCO3的含量:取200g水垢,加入过量的稀盐酸,同时测量5分钟内生成气体的质量.结果如下表:| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 质量/g | 30 | 50 | 60 | 66 | 66 |
(1)4分钟后,产生的CO2不再增加,说明水垢中CaCO3
(2)当反应完全时,CaCO3消耗的氯化氢为
(3)该水垢中CaCO3的质量分数是多少?
分析:根据化学反应的实质探究物质的组成:当二氧化碳的量不再增加时说明混合物中的碳酸钙已全部参与反应,根据得到的二氧化碳的质量即可求出混合物中碳酸钙的质量和消耗的氯化氢的质量.
解答:解:(1)4分钟后,产生的CO2不再增加,说明水垢中CaCO3已全部反应,故答案为:已
(2)由图不难看出,共得到二氧化碳66克,根据二氧化碳的质量即可求出参与反应的氯化氢的质量和碳酸钙的质量.
解:设碳酸钙消耗的氯化氢的质量为x,200g水垢中碳酸钙的质量是y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
y x 66g
=
x=
=109.5g
=
y=
=150g
水垢中碳酸钙的质量分数为:
×100%═75%
答:水垢中碳酸钙的质量分数为75%.
(2)由图不难看出,共得到二氧化碳66克,根据二氧化碳的质量即可求出参与反应的氯化氢的质量和碳酸钙的质量.
解:设碳酸钙消耗的氯化氢的质量为x,200g水垢中碳酸钙的质量是y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
y x 66g
| 73 |
| 44 |
| x |
| 66g |
| 73×66g |
| 44 |
| 100 |
| 44 |
| y |
| 66g |
| 100×66g |
| 44 |
水垢中碳酸钙的质量分数为:
| 150g |
| 200g |
答:水垢中碳酸钙的质量分数为75%.
点评:主要考查了化学方程式的计算,培养学生的计算能力和解决问题的能力.

练习册系列答案
相关题目
长久使用的热水瓶底部有一层水垢,主要成分是碳酸钙,用稀盐酸可以清除水垢.某学校化学课外兴趣小组的同学通过实验测定水垢中碳酸钙的含量,将过量的稀盐酸加到200g水垢中,同时测量4分钟内产生CO2的质量部分结果如下表:[CaCO3+2HCl═CaCl2+H2O+CO2↑]
(1)该小组因故没有记录反应时间为180s时的数
据M.你由表中数据推测,M= g.
(2)反应生成CO2的总质量为 g.(3)根据实验数据,在右边的坐标纸上绘制生成CO2质量与反应时间关系的曲线.你由曲线中推测在反应60s时,生成CO2的质量约为 .
(4)计算水垢中碳酸钙质量分数是多少?
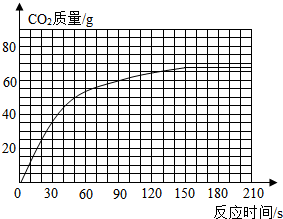
| 时间/s | 30 | 50 | 90 | 150 | 180 | 210 |
| CO2质量/g | 30 | 50 | 60 | 66 | M | 66 |
据M.你由表中数据推测,M=
(2)反应生成CO2的总质量为
(4)计算水垢中碳酸钙质量分数是多少?

长久使用的热水瓶底部有一层水垢,主要成分是CaCO3和Mg(OH)2,某学校化学研究小组的同学通过实验测定水垢中CaCO3的含量:取200g水垢,加入过量的稀盐酸,同时测量5分钟内生成气体的质量,结果如下表:
试回答下列问题:
(1)4分钟后,产生的CO2不再增加,说明水垢中CaCO3 (填已或未)反应完全?
(2)该水垢中CaCO3的质量分数是多少?
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 质量/g | 30 | 50 | 60 | 66 | 66 |
(1)4分钟后,产生的CO2不再增加,说明水垢中CaCO3
(2)该水垢中CaCO3的质量分数是多少?
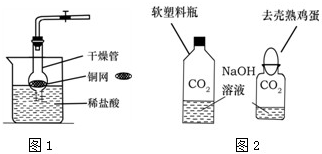 CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质:
CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质: