题目内容
长久使用的热水瓶底部有一层水垢,主要成分是碳酸钙,用稀盐酸可以清除水垢.某学校化学课外兴趣小组的同学通过实验测定水垢中碳酸钙的含量,将过量的稀盐酸加到200g水垢中,同时测量4分钟内产生CO2的质量部分结果如下表:[CaCO3+2HCl═CaCl2+H2O+CO2↑]| 时间/s | 30 | 50 | 90 | 150 | 180 | 210 |
| CO2质量/g | 30 | 50 | 60 | 66 | M | 66 |
据M.你由表中数据推测,M=
(2)反应生成CO2的总质量为
(4)计算水垢中碳酸钙质量分数是多少?
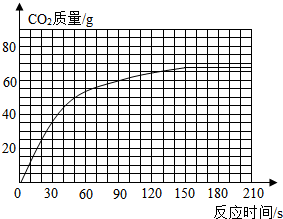
分析:(1)通过分析表格中二氧化碳的质量随时间的变化来解答.
(2)通过分析表格中二氧化碳的质量随时间的变化来解答.
(3)根据表格中所给数据进行大约描点连接.
(4)根据生成的二氧化碳的质量,有化学方程式计算出反应的碳酸钙的质量,进而求出质量分数.
(2)通过分析表格中二氧化碳的质量随时间的变化来解答.
(3)根据表格中所给数据进行大约描点连接.
(4)根据生成的二氧化碳的质量,有化学方程式计算出反应的碳酸钙的质量,进而求出质量分数.
解答:解:根据表格可看出150秒时二氧化碳质量为66克,210秒时质量也是66克,所以可以得出结论150秒时反应已经完成,生成的二氧化碳的最大量是66克.
故答案为:(1)66;(2)66
(3)根据表格知图象有几个关键点,即(30,30),(50,50),(90,60),150秒以后二氧化碳的质量为定值,
故曲线图如下,由图象可看出60秒时大约生成二氧化碳质量为53g.故答案为:53g
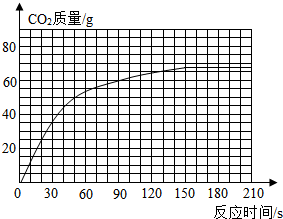
(4)[解]设:碳酸钙质量为x..
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 66g
=
解之得:x=150g
所以碳酸钙的质量分数=
×100%=75%
答:碳酸钙质量分数为75%.
故答案为:(1)66;(2)66
(3)根据表格知图象有几个关键点,即(30,30),(50,50),(90,60),150秒以后二氧化碳的质量为定值,
故曲线图如下,由图象可看出60秒时大约生成二氧化碳质量为53g.故答案为:53g

(4)[解]设:碳酸钙质量为x..
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 66g
| 100 |
| x |
| 44 |
| 66g |
解之得:x=150g
所以碳酸钙的质量分数=
| 150g |
| 200g |
答:碳酸钙质量分数为75%.
点评:本题综合性比较强,既考查了学生运用数学知识解决化学问题的能力,又考查了学生利用化学方程式进行计算的能力.

练习册系列答案
 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
长久使用的热水瓶底部有一层水垢,主要成分是CaCO3和Mg(OH)2,某学校化学研究小组的同学通过实验测定水垢中CaCO3的含量:取200g水垢,加入过量的稀盐酸,同时测量5分钟内生成气体的质量.结果如下表:
试回答下列问题:
(1)4分钟后,产生的CO2不再增加,说明水垢中CaCO3 (填已或未)反应完全?
(2)当反应完全时,CaCO3消耗的氯化氢为 g.
(3)该水垢中CaCO3的质量分数是多少?
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 质量/g | 30 | 50 | 60 | 66 | 66 |
(1)4分钟后,产生的CO2不再增加,说明水垢中CaCO3
(2)当反应完全时,CaCO3消耗的氯化氢为
(3)该水垢中CaCO3的质量分数是多少?
长久使用的热水瓶底部有一层水垢,主要成分是CaCO3和Mg(OH)2,某学校化学研究小组的同学通过实验测定水垢中CaCO3的含量:取200g水垢,加入过量的稀盐酸,同时测量5分钟内生成气体的质量,结果如下表:
试回答下列问题:
(1)4分钟后,产生的CO2不再增加,说明水垢中CaCO3 (填已或未)反应完全?
(2)该水垢中CaCO3的质量分数是多少?
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 质量/g | 30 | 50 | 60 | 66 | 66 |
(1)4分钟后,产生的CO2不再增加,说明水垢中CaCO3
(2)该水垢中CaCO3的质量分数是多少?
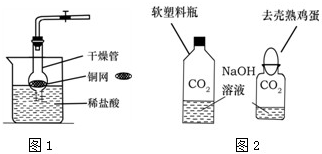 CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质:
CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质: