题目内容
【题目】某氢氧化钙中含有碳酸钙杂质,称取研细的该样品12.4g放入锥形瓶中,加入32.6g水,充分振荡后形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生,此时消耗盐酸的总质量为37.5g,锥形瓶中剩余物质的质量为80.3g。
(1)反应产生二氧化碳的质量为______g。
(2)求样品中氢氧化钙的质量分数_____(写出计算过程,结果精确到0.1%)。
【答案】2.2 59.7%
【解析】
(1)反应产生二氧化碳的质量为:12.4g+32.6g+37.5g-80.3g=2.2g,
故填:2.2.
(2)设样品中碳酸钙质量为x,
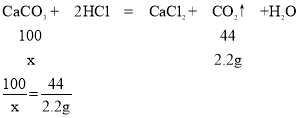
x=5g,
样品中氢氧化钙的质量分数为:![]() ×100%=59.7%,
×100%=59.7%,
答:样品中氢氧化钙的质量分数为59.7%.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目