题目内容
【题目】内江拥有中国西南地区最大的再生资源基地,可回收处理大量废旧塑料电器及玻璃等,某品牌电器的废旧电路板中还有Fe、Cu、Ag、Ni(镍,银白色金属) 等金属,如下图是某车间回收部分金属的工艺流程,已知:![]() 。回答下列问题。
。回答下列问题。
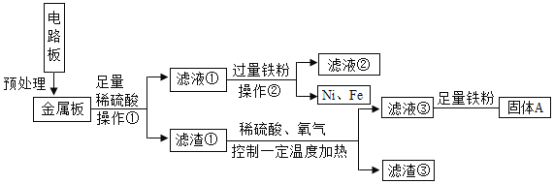
(1)操作①的名称为_______;
(2)滤渣③中含有的金属是_______;
(3)根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱顺序是Ni _____Fe(填 “>”或“<”);
(4)滤液③中加入足量铁粉的主要目的是_____,在这个过程中一定涉及的反应方程式为___________;
(5)相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点是______。
【答案】过滤 Ag < 将铜全部置换出来 Fe+CuSO4=FeSO4+Cu 避免了焚烧产生的污染性气体,更加的环保(答案合理即可)。
【解析】
(1)操作①是将滤液和滤渣分开,而过滤操作可以将不溶性固体从溶液中分离出来,所以操作①是过滤。故填:过滤。
(2)铜银和稀硫酸不反应,铁镍和稀硫酸反应,滤渣中的铜、氧气和稀硫酸在加热的条件下生成硫酸铜和水,银不反应,所以滤渣③中含有的金属是Ag;故填:Ag。
(3)加入过量的铁后,得到的滤渣中含有铁和镍,所以可以得出Ni、Fe的金属活动性强弱顺序是Ni<Fe;故填:<。
(4)铁的活动性排在铜的前面,加入的铁能将硫酸铜中的铜置换出来,所以在滤液③中加入足量铁粉的主要目的是:将铜全部置换出来;铁加入后和硫酸铜反应生成铜和硫酸亚铁,反应的化学方程式为:Fe+CuSO4=FeSO4+Cu。故填:将铜全部置换出来;Fe+CuSO4=FeSO4+Cu。
(5)直接焚烧废旧电路板会产生污染性气体,而该工艺主要则避免了焚烧产生的污染,更加的环保。故填:避免了焚烧产生的污染性气体,更加的环保(答案合理即可)。

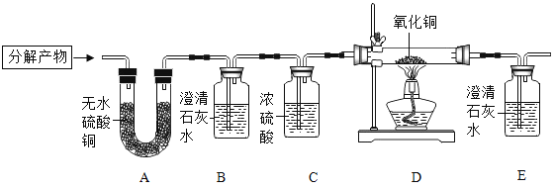
【题目】某校实验室有一瓶久置的铁屑,其成分是铁、氧化铁和水。为测定其中各成分的质量分数,某兴趣小组按下图所示装置进行实验(装置气密性良好;固定装置已略去;氮气不与铁屑中的成分反应;碱石灰是氧化钙和氢氧化钠的混合物)。
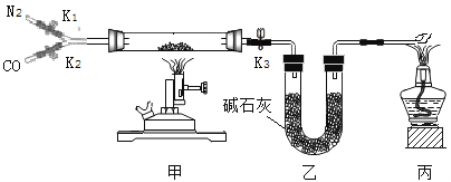
部分实验步骤如下:
Ⅰ.称量硬质玻璃管的质量。将样品放入硬质玻璃管中,称量硬质玻璃管和样品的质量。
II.连接好装置。缓缓通入N2,点燃甲处的酒精喷灯,待硬质玻璃管中固体恒重,记录硬质玻璃管和剩余固体的质量。
Ⅲ.再次连接好装置,继续实验。通入CO,点燃丙处的酒精灯和甲处的酒精喷灯。待硬质玻璃管中固体恒重,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却。再次记录硬质玻璃管和剩余固体的质量。
实验数据记录如下表:
硬质玻璃管 | 硬质玻璃管和样品 | 步骤II硬质玻璃 管和剩余固体 | 步骤步骤Ⅲ硬质玻璃 管和剩余固体 | |
质量 | m1 | m2 | m3 | m4 |
请回答下列问题:
(1)步骤Ⅲ丙处酒精灯的作用是____________。
(2)步骤Ⅲ硬质玻璃管中反应的化学方程式为________。
(3)样品中氧化铁的质量分数为_____(用m1、m2、m3、m4的代数式表示)。若步骤Ⅲ中氧化铁没有完全反应,样品中水的质量分数测量结果将______(填“偏大”“偏小”或“不变”)。
(4)有关样品,下列说法正确的是_____(填字母标号)。
A样品中氢元素的质量为1/9(m2-m3) B样品中铁单质和氧化铁的质量总和为m3-m1
C样品中铁单质的质量为m4-m1 D样品中氧元素的质量为m3-m4
【题目】化学兴趣小组的同学对酒精的组成进行了以下探究:
(1)点燃前,观察到酒精是无色透明液体,有特殊香味,这是指酒精的__________(填“物理性质”或“化学性质”)。
(2)同学们想探究酒精的组成元素,设计并进行了如下实验探究。
步骤 | 操作 | 现象 | 分析 | 结论 |
步骤一 | 点燃酒精灯,在火焰上方罩一个冷而干燥的烧杯。 | 烧杯内壁出现_______。 | 酒精燃烧生成了水。 | 酒精中含有_____元素 |
步骤二 | 将上步的烧杯迅速翻转,倒入适量澄清石灰水,并振荡。 | 澄清石灰水变浑浊。 | 酒精燃烧生成了______。 | 酒精中含有碳元素 |
(归纳结论)①酒精由碳、氢元素组成;
②酒精完全燃烧的文字表达式为:______________。
(反思评价)老师指出,同学们的本实验结论不合理,原因是:_____________。
(拓展探究)老师建议:量取一定质量的酒精,让其在足够的氧气中充分燃烧,然后再分别精确测量所生成的水和二氧化碳的质量,即可得出正确结论。老师的依据是:____________。