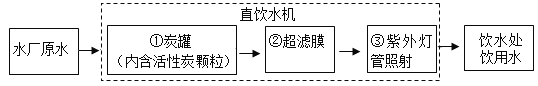
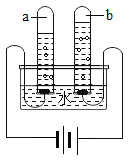
题目内容
【题目】下图是某化学兴趣小组的同学们配制100 g溶质质量分数为11%的NaCl溶液的有关实验。
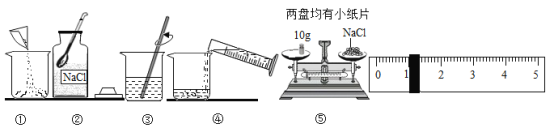
(1)用图中序号表示配制该溶液的正确操作顺序为_____;
(2)下列会导致所得溶液中溶质质量分数偏小的选项(假设每一项其他步骤操作正确)是_____(填序号);
A 氯化钠固体不纯
B 用量筒量取水时俯视读数
C 装瓶时有少量溶液洒出
D 溶解时烧杯内壁有水珠
(3)某同学用如图⑤的方法称取所需食盐,若要保证所配食盐水中溶质质量分数不变,该同学应量取水的体积约为_____mL;
(4)刘同学欲用上述配制好的氯化钠溶液再配制3%的氯化钠溶液,配制过程中的操作步骤为:计算、_____、_____、装瓶贴签。
【答案】②⑤①④③ AD 72.8 量取 稀释
【解析】
(1)配制溶液的操作步骤是:计算、称量、溶解、装瓶存放,用图中序号表示配制该溶液的正确操作顺序为②⑤①④③;
(2)A、氯化钠固体不纯,导致溶质的质量偏少,质量分数偏小;
B、用量筒量取水时俯视读数,读数偏大,实际量取溶剂的量偏少,溶质的质量分数偏大;
C、装瓶时有少量溶液洒出,溶液具有均一性,溶质的质量分数不变;
D、溶解时烧杯内壁有水珠,溶剂的量偏多,溶质的质量分数偏小;
故选AD;
(3)称量一定质量的固体时,若物质与砝码反放了,会导致实际称量的物质质量=砝码的质量-游码的质量=10g-1g=9g,若要保证所配食盐水中溶质质量分数不变,溶液的质量为9g÷11%≈81.8g,该同学应量取水的质量约为:81.8g-9g=72.8g,体积约为72.8mL;
(4)欲用上述配制好的氯化钠溶液再配制3%的氯化钠溶液,配制过程中的操作步骤为:计算、量取、稀释、装瓶贴签。

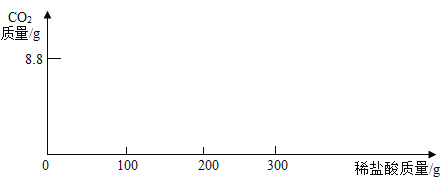
【题目】某研究性学习小组称取含NaCl的Na2CO3固体25 g,将其配制成溶液,再向其中逐滴加入足量的7.3%的稀盐酸,使气体完全放出,共收集到 8.8 g CO2气体。
(1)计算原固体中Na2CO3的质量分数____________和消耗稀盐酸的总质量____________(写出计算过程)。
(2)下表为研究性学习小组向上述配制的混合液中分三次逐滴加入(边加边振荡)稀盐酸后所记录的部分数据。经查阅资料知Na2CO3与HCl反应可以分两步进行:Na2CO3+HCl=NaCl+NaHCO3,NaHCO3+HCl=NaCl+H2O+CO2↑。
①请完成表格中未填的部分。
实验次数 | 每次产生的CO2的质量/g |
第一次先逐滴滴加稀盐酸100 g | ________ |
第二次再逐滴滴加稀盐酸100 g | 8.8 |
第三次再逐滴滴加稀盐酸100 g | 0 |
②根据表中数据在坐标系中画出CO2的质量(纵坐标)与所加入稀盐酸的质量(横坐标)的关系图________。