题目内容
【题目】请根据如图所示的实验装置填空。

(1)仪器②的名称是_______________;实验室用B装置制备氧气时,仪器①所装药品的名称是_______________。
(2)现有大理石颗粒、小苏打粉末、稀盐酸、稀硫酸,选择合适的物质用C装置制备CO2 气体;其化学方程式为_______________;使反应停止的操作方法是_______________。
(3)实验室常用加热醋酸钠和碱石灰的固体混合物来制备甲烷气体。甲烷无色无味,密度比空气小,极难溶于水,则制备并收集甲烷可用图中的______________(填字母标号)装置组合。若改用下图“装置甲”收集甲烷,气体应从__________端导入 (选填“a” 或“b”)。
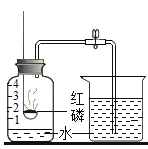
(4)实验室常将锌粒和盐酸反应生成的气体通过右图“装置乙”比而得到较纯净的氢气,发生反应的化学方程式为_______________;设置A瓶的目的是除去气体中含有的______________(填名称)。B中的“某液体”是______________(填名称),其作用是_______________。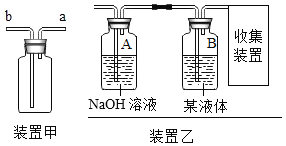
【答案】集气瓶 过氧化氢 ![]() 关闭活塞 AD (或AF) a
关闭活塞 AD (或AF) a ![]() 氯化氢 浓硫酸 除去氢气中的水蒸气。
氯化氢 浓硫酸 除去氢气中的水蒸气。
【解析】
(1)仪器②的名称是集气瓶;实验室用B装置制备氧气时,只能是过氧化氢溶液和二氧化锰制取氧气,仪器①所装液体药品的名称是过氧化氢溶液。
(2)可以选择大理石颗粒、稀盐酸用C装置制备CO2 气体;其化学方程式为![]() ;使反应停止的操作方法是:关闭活塞,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止。
;使反应停止的操作方法是:关闭活塞,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止。
(3)实验室常用加热醋酸钠和碱石灰的固体混合物来制备甲烷气体。发生装置是固体加热型,甲烷密度比空气小,极难溶于水,收集装置是排水法和向下排空气法,则制备并收集甲烷可用图中的AD (或AF) 装置组合。若改用下图“装置甲”收集甲烷,气体应从a端导入。
(4)实验室常将锌粒和盐酸反应生成的气体通过右图“装置乙”比而得到较纯净的氢气,锌粒和盐酸反应生成氯化锌和氢气,反应的化学方程式为![]() ;设置A瓶的目的是除去气体中含有的氯化氢。B中的“某液体”是浓硫酸,其作用是:除去氢气中的水蒸气。
;设置A瓶的目的是除去气体中含有的氯化氢。B中的“某液体”是浓硫酸,其作用是:除去氢气中的水蒸气。

【题目】小思在实验室发现一瓶瓶塞破损的淡黄色固体,标签标明该固体是过氧化钠。该固体是否已经变质?于是他和同学们进行了以下实验探究:
[查阅资料]
过氧化钠(化学式为Na2O2)是一种淡黄色固体,常用在呼吸面具和潜水中制氧气,其原理为:
2Na2O2+2CO2═2Na2CO3+O2
2Na2O2+2H2O═4NaOH+O2↑
[分析猜想]美奇同学根据观察并结合所给资料判断。该固体中一定还含有Na2O2,理由是_____。
他进一步对固体成份提出了以下猜想:
①只含Na2O2②含Na2CO3和Na2O2两种物质
③含Na2CO3、NaOH两种物质 ④含Na2O2、Na2CO3和NaOH三种物质
[问题分折]请你说明提出猜想③的依据是_____。
[实验探究]为确定该固体的成份,他们又进行了如下实验:
实验方案与步骤 | 实验现象 | 实验结论 |
①取一定量固体于试管中,加入足量蒸馏水,并将带火星木条伸入试管内 | 现象:有气泡产生,木条燃烧程度增强 | 固体中含有Na2O2. |
②将①所得溶液平均分为两份,向第一份溶液中加入足量稀盐酸 | 现象:_____ | 固体中含Na2CO3 |
③向第二份溶液中加入过量的BaCl2溶液,充分反应后取上层清液滴入无色酚酞 | (1)产生白色沉淀;(2)溶液变红 | 固体中含有NaOH |
请写出实验③中产生白色沉淀的化学方程式:_____。
[反思与交流]
有同学认为通过定量计算可确定固体中是否含有NaOH.具体方案如下:①取一定量固体加入到足量的水中,测定产生氧气的质量。②向①中加入足量的CaCl2溶液,通过_____、洗涤、干燥称量产生沉淀质量,进而计算出固体中含Na2CO3的质量。③判断固体中是否含有NaOH。