题目内容
【题目】有一包固体粉末,可能有CuSO4、CaCO3、Na2SO4中的一种或几种所组成,小文为了确定它的成分,进行了如下实验:
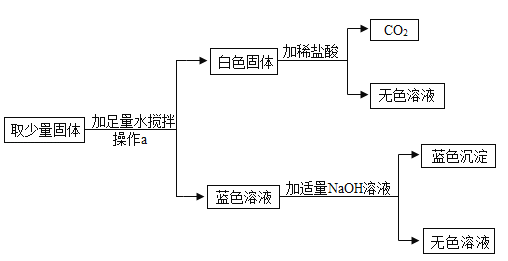
(1)操作a的名称是_____,其中必须要用到的玻璃仪器有烧杯、玻璃棒和_____.
(2)白色固体是_____,它与盐酸反应所属基本反应类型为_____.
(3)小文通过实验后认为,这包固体粉末中只有两种物质,他的判断是_____(填“正确”或“错误”)的,理由是_____.
【答案】过滤 漏斗 CaCO3 复分解反应 错误 无法判断是否存在Na2SO4
【解析】
(1)操作a得到难溶性固体和蓝色溶液,是过滤,需要的仪器有:铁架台、烧杯、玻璃棒和漏斗,其中缺少的玻璃仪器是漏斗(带滤纸,用于过滤);
(2)白色固体是难溶性的碳酸钙,化学式为:CaCO3;稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,故反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;该反应是酸和盐发生的复分解反应;
(3)小文通过实验后认为,这包固体粉末中只有两种物质,他的判断是错误的,理由是:白色沉淀加入稀盐酸有二氧化碳气体,说明一定含有碳酸钙,固体加水搅拌产生蓝色溶液,说明一定有硫酸铜,而硫酸钠不影响实验的现象,所以可能含有硫酸钠,故无法判断是否存在Na2SO4。

练习册系列答案
相关题目