题目内容
【题目】下列四个图像分别对应四个变化过程,其中错误的是
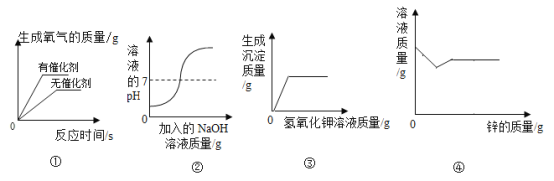
A.①表示用两份等质量、等浓度的过氧化氢溶液分别制取氧气
B.②表示向一定体积的稀盐酸中逐滴加入足量的氢氧化钠溶液
C.③表示向一定量的氯化铁和稀盐酸的混合溶液中,逐滴加入氢氧化钾溶液至过量
D.④表示向硝酸银和硝酸铜的混合溶液中加入足量的锌粉
【答案】AC
【解析】
A、催化剂只改变反应速率,但不影响生成氧气的质量,用两份等质量、等浓度的过氧化氢溶液分别制取氧气,最后所得氧气的质量应该相等,符合题意;
B、稀盐酸显酸性,溶液的pH<7,稀盐酸与氢氧化钠溶液反应生成氯化钠和水,加入足量氢氧化钠溶液后,溶液pH逐渐增大直至大于7,不符合题意;
C、氢氧化钾先与稀盐酸反应生成氯化钾和水,此时无沉淀产生,当稀盐酸消耗完后,氢氧化钾再与氯化铁反应生成氢氧化铁沉淀和氯化钾,故曲线起点不在原点,符合题意;
D、向硝酸银和硝酸铜的混合溶液中加入足量的锌粉,根据金属的活动性顺序,锌粉先和硝酸银反应,待硝酸银反应完全后,锌再与硝酸铜反应,锌与硝酸银反应生成硝酸锌和银,化学方程式为:![]() ,消耗65份的锌可以得到216份银,固体质量增加,溶液质量减小,硝酸银完全反应后,锌与硝酸铜反应生成硝酸锌和铜,化学方程式为:
,消耗65份的锌可以得到216份银,固体质量增加,溶液质量减小,硝酸银完全反应后,锌与硝酸铜反应生成硝酸锌和铜,化学方程式为:![]() ,消耗65份锌可以得到64份铜,固体质量减小,溶液质量增加,因此随着反应的进行,溶液质量先减小再增大,恰好反应后,溶液质量不再变化,不符合题意。
,消耗65份锌可以得到64份铜,固体质量减小,溶液质量增加,因此随着反应的进行,溶液质量先减小再增大,恰好反应后,溶液质量不再变化,不符合题意。
故选AC。

 阅读快车系列答案
阅读快车系列答案【题目】在学校学习有关酸、碱的化学性质后,马丁组织同学们用生活中的常见物品探究酸的性质。
(实验用品)醋精、食品干燥剂、鸡蛋壳、牵牛花花瓣、生锈铁钉、纯碱、pH试纸、木筷子。
(查阅资料)
①醋精中含有10%~15%的醋酸,呈无色。
②食品干燥剂的主要成分为氧化钙,鸡蛋壳的主要成分为碳酸钙。
③牵牛花汁液在酸性溶液中呈红色,中性溶液中呈紫色,碱性溶液中呈蓝色。
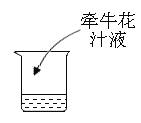
(实验方案)取等量醋精于烧杯中,分别进行如下操作:
实验1 | 实验2 | 实验3 | 实验4 | |
实验操作 |
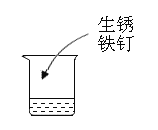
|
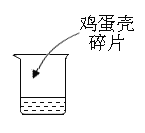
|
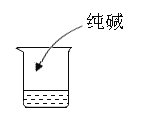
|
|
实验现象 | 溶液变红 | 溶液变为浅黄色,一段时间后,有气泡产生 | 有气泡产生 | 有气泡产生 |
(解释与结论)
(1)实验1说明_______________。
(2)实验2中观察到有气泡产生的原因是____________。
(3)实验3可得到的结论是__________。
(4)实验4能否证明酸能与碱发生反应并说明原因是_________
(反思与评价)
(5)验证实验3和4生成气体是二氧化碳的实验是:_________。
(6)若向配制好的碱溶液中滴入牵牛花汁液,然后逐滴滴加醋精,边滴加边振荡,观察到_____,证明酸能与碱反应。
【题目】某实验小组的同学在做酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中加入一定量的稀硫酸后,发现忘了滴加酸碱指示剂。因此,他们停止滴加稀硫酸,并对烧杯内溶液中的溶质成分进行了探究。
[提出问题]该烧杯内溶液中的溶质是什么?
[猜想假设]猜想一:只有Na2SO4;
猜想二:___________________________。
猜想三:含有Na2SO4和NaOH。
[查阅资料]硫酸钠溶液呈中性。
[进行实验]同学们设计了如下不同的实验方案,证明猜想二是成立的。请你帮他们填写有关实验步骤或实验现象。
方案 | 实验步骤 | 实验现象 |
方案一 | 取少量烧杯中的溶液于试管中,加入紫色石蕊溶液 | ___________________________。 |
方案二 | 取少量__________________于试管中,加入一定量的烧杯中的溶液 | 固体溶解,溶液变为黄色 |
方案三 | 取少量烧杯中的溶液于另- -支试管中,加入氯化钡溶液 | ___________________________。 |
方案四 | ___________________________。 | 产生气泡. |
[反思交流]
(1)上述方案有一个不合理,请指出并说明理由___________________________。
(2)方案二中反应的化学方程式为___________________________。