题目内容
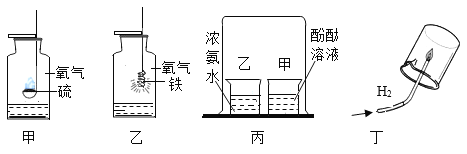
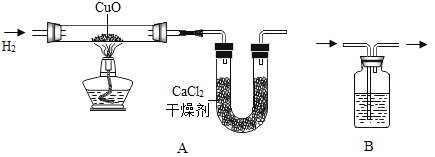
【题目】用H2和CuO反应的实验来测定水的组成,如图A所示。请回答下列问题:
(1)实验中,用锌粒和稀硫酸反应制取氢气:
①检验氢气纯度后,先通一段时间氢气,再加热CuO进行反应,其主要目的是_______;
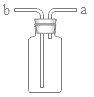
②与CuO反应前,应将制取的H2通过图B所示装置进行干燥,其中所盛的试剂是_______;
(2)实验中,测定的数据如表所示,根据数据计算生成的水中氢氧元素的质量比为:_____(要求有计算式)
实验前 | 实验后 | |
CuO和玻璃管总质量 | 65.6g | 59.2g |
CaCl2和U形管的总质量 | 100.8g | 108.0g |
(3)下列情况下,对实验测定结果一定没有影响的是_______(填序号)
①相对CuO而言,H2是过量的②CuO粉末中含有不与H2反应的杂质③反应中部分CuO变成Cu2O④干燥剂CaCl2有部分失效⑤用固体NaOH代替CaCl2做干燥剂
【答案】赶走玻璃管中的空气,防止发生爆炸 浓硫酸 m(H):m(O)=[(108.0g-100.8g)-(65.6g-59.2g)]:(65.6g-59.2g)=1:8 ①③
【解析】
(1)①凡是可燃性气体都能与空气混合可能发生爆炸,所以加热前先要排净装置内的空;②氢气可以用浓硫酸干燥;
(2)玻璃管中的反应为氧化铜和氢气反应,生成水和铜单质,据题意及质量守恒定律,知道玻璃管与氧化铜的质量差是水中氧的质量,而U形管与氯化钙的质量差是水的质量,水的质量减氧的质量即为氢的质量。故氧、氢元素的质量之比为m(H):m(O)=[(108.0g-100.8g)-(65.6g-59.2g)]:(65.6g-59.2g)=1:8。
(3)由(2)的算式可以看出氢气的量及氧化铜是否变成氧化亚铜对于结果无影响,而②的杂质如果是能与氧化铜反应的物质则对结果会有影响,失效的氯化钙会对水的吸收不充分,使结果不准确,用氢氧化钠做干燥剂时也会吸收空气中的二氧化碳而使结果不准确。故选①③。

 名校课堂系列答案
名校课堂系列答案【题目】某校化学兴趣小组在学习了催化剂的知识后,想探究氧化铜能否在过氧化氢溶液分解反应中起到催化作用。请你一起参与他们的探究过程,并完成下列填空。
(提出问题)CuO能不能作过氧化氢溶液分解反应的催化剂呢?
(做出猜想)CuO能作过氧化氢溶液分解反应的催化剂。
(实验验证)
实验 | 实验步骤 | 实验现象 | 实验结论 |
实验一 | 在试管中加入少量的H2O2溶液,然后将带火星的木条伸入试管中 | __________ | 常温下H2O2溶液分解速率非常缓慢,放出极少量的氧气 |
实验二 | 在装有等量H2O2溶液的试管中加入少量的CuO,然后将带火星的木条伸入试管中 | 有较多气泡产生,木条复燃 | ___________ |
(讨论与反思)经过讨论,有的同学认为只有上述两个实验,不能证明CuO能作过氧化氢溶液分解反应的催化剂,还要补充一个探究实验。
实验三:
(实验目的)探究在反应前后CuO的质量是否发生改变。
(实验步骤)①准确称量CuO(少量)的质量;
②重复实验二的步骤,待反应结束后,将试管里的物质过滤,洗涤,干燥,称重;
③对比反应前后CuO的质量。
(讨论交流)如果_________,则说明CuO能作过氧化氢溶液分解反应的催化剂。但小华认为,要证明猜想,上述三个实验还不足以说明,还需要再增加一个实验。
(实验目的)_________
(实验结论)CuO能作过氧化氢溶液分解反应的催化剂,请写出CuO催化过氧化氢溶液分解的文字表达式:____________。