题目内容
【题目】小红和小蓝两同学玩“点灯”游戏,规则如下:小红选择一盏灯﹣﹣﹣红灯A,其余5盏灯内的物质若能与A反应,则也变为红灯。小蓝在未变红的灯内选择一盏灯﹣﹣﹣蓝灯B,B若能跟其它灯内物质反应,则与之反应的灯变为蓝灯,若最后蓝灯数量多,则小蓝胜出,若最后红灯数量多,则小红胜出。(灯内物质除Fe、CO外,其余均为溶液)
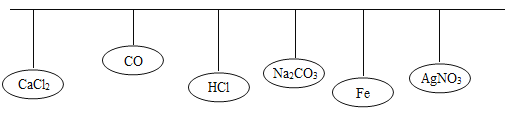
若A为HCl,点亮了3盏红灯,而小蓝选择了剩余灯中的1盏,并将两盏红灯转化为蓝灯,最后3:2取胜。
(1)小蓝同学选择的蓝灯B是_____,写出B将两盏红灯转化为蓝灯相应的化学方程式_____、_____。
(2)如果小红开始选择的A是碳酸钠,小蓝想赢,则B为_____。
(3)从策略上讲,如果想赢,小红开始选择的灯A应该是_____。
【答案】CaCl2 CaC12+2AgNO3=Ca(NO3 )2+2AgCl↓ CaCl2+Na2 CO3=CaCO3↓+2NaCl Fe AgNO3
【解析】
由于小红选择盐酸作为红灯,所以碳酸钠、铁和硝酸银都转化为红灯,而剩余的灯只有氯化钙和一氧化碳,所以小蓝同学选择的蓝灯B是 CaCl2,而不是一氧化碳,因为一氧化碳不能和其他物质反应。则氯化钙和碳酸钠反应生成碳酸钙和氯化钠,氯化钙和硝酸银反应生成硝酸钙和氯化银。
(1)由于小红选择盐酸作为红灯,所以碳酸钠、铁和硝酸银都转化为红灯,而剩余的灯只有氯化钙和一氧化碳,所以小蓝同学选择的蓝灯B是 CaCl2,而不是一氧化碳,因为一氧化碳不能和其他物质反应。则氯化钙和碳酸钠反应生成碳酸钙和氯化钠,氯化钙和硝酸银反应生成硝酸钙和氯化银,对应的化学方程式为
![]()
(2)如果小红开始选择的A是碳酸钠,则红灯有氯化钙、盐酸和硝酸银,则不变红有一氧化碳和铁,小蓝想赢,则B为 Fe,会导致盐酸和硝酸银变成蓝色,所以有铁、盐酸以及硝酸银三个蓝灯,而红灯只有碳酸钠、氯化钙,所以是小蓝赢。
(3)从策略上讲,如果想赢,那就要尽可能剩余物质不能和自己选择的物质反应,所以小红开始选择的灯A应该是 AgNO3,这样剩余的只有一氧化碳,且一氧化碳和其他物质不反应,小蓝只能选择一氧化碳,且一氧化碳也不能使其他变蓝。

【题目】化学兴趣小组探究金属的性质时,将一段去除氧化膜的镁条,放入一定量的稀盐酸中,有气泡产生,充分反应后静置,发现试管中有灰白色沉淀。写出产生气泡的反应化学方程式______。
(提出问题)灰白色沉淀是什么物质?
(猜想假设)①小华认为灰白色沉淀为碳酸镁(MgCO3),其他同学认为不需要实验就能否定小华的猜想,理由是_____________________。
②小宇认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体。
③小彤认为灰白色沉淀为__________________。
(实验探究1)
实验操作 | 现象 | 结论 |
①取试管中的上层清液,加入适量的氯化镁固体 | 氯化镁固体__(选填“溶解”或“不溶解”) | 小宇猜想错误 |
②取适量白色沉淀加入足量稀盐酸中 | 没有气泡冒出 | 小彤猜想错误 |
基于以上探究与分析,原有猜想均遭到了否定。
(查阅资料)
HCl+AgNO3═HNO3+AgCl↓,AgCl是一种白色沉淀。氯化氢是酸性气体,能使蓝色石蕊试纸变红。进行
(实验探究2)
他们又另取灰白色沉淀放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了__气体。如何检验这种气体_______(实验步骤、现象、结论)。
同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的过程,从而生成了碱式氯化镁沉淀。据文献介绍,碱式氯化镁存在多种组成结构,化学通式可表示为Mgx(OH)yClzmH2O(其中2x﹣y﹣z=0,0≤m≤6)。
(反思拓展)
(1)做镁与稀盐酸反应的实验时,为了不让试管中出现灰白色沉淀,镁条的用量_______。
(2)铁片和铜片放入稀硫酸中产生的现象也不相同,据此推测出铁的活动性比铜_____。