题目内容
【题目】现有一瓶硫酸溶液,为测定其溶质的质量分数,取该溶液98g于烧杯中,逐渐加入足量的氯化钡溶液,反应中物质间的质最关系如图所示。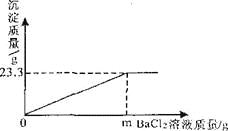
请计算:
(1)原硫酸溶液中溶质的质量分数__________。
(2)若取一定量该硫酸溶液配制50g溶质的质量分数为7%的稀硫酸,需加入水的质量是多少g?_________
【答案】l0% l5g
【解析】
由图可知,生成硫酸钡沉淀的质量为23.3g;
(1)设:98g稀硫酸中含硫酸质量为x。
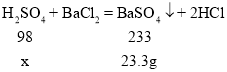
![]() x=9.8g
x=9.8g
该硫酸溶液中溶质的质量分数![]()
(2)设:配制溶质质量分数为7%的硫酸溶液50g,需用溶质质量分数为10%的硫酸溶液的质量是y
50g×7%=y·10% 解得y=35g
需加入水的质量是50g-35g=15g
答:(1)原硫酸溶液中溶质的质量分数为l0%;
(2)需加入水的质量是l5g。

 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案【题目】化学兴趣小组的同学对酒精的组成进行了以下探究:
(1)点燃前,观察到酒精是无色透明液体,有特殊香味,这是指酒精的__________(填“物理性质”或“化学性质”)。
(2)同学们想探究酒精的组成元素,设计并进行了如下实验探究。
步骤 | 操作 | 现象 | 分析 | 结论 |
步骤一 | 点燃酒精灯,在火焰上方罩一个冷而干燥的烧杯。 | 烧杯内壁出现_______。 | 酒精燃烧生成了水。 | 酒精中含有_____元素 |
步骤二 | 将上步的烧杯迅速翻转,倒入适量澄清石灰水,并振荡。 | 澄清石灰水变浑浊。 | 酒精燃烧生成了______。 | 酒精中含有碳元素 |
(归纳结论)①酒精由碳、氢元素组成;
②酒精完全燃烧的文字表达式为:______________。
(反思评价)老师指出,同学们的本实验结论不合理,原因是:_____________。
(拓展探究)老师建议:量取一定质量的酒精,让其在足够的氧气中充分燃烧,然后再分别精确测量所生成的水和二氧化碳的质量,即可得出正确结论。老师的依据是:____________。
【题目】2011年5月1日开始,对醉酒驾车者一律刑事拘留。下表是国家对“饮酒驾车”和“醉酒驾车”的界定标准:
饮酒驾车 | 20毫克/100毫升 ≤ 血液中的酒精含量 < 80毫克/100毫升 |
醉酒驾车 | 驾车血液中的酒精含量 ≥ 80毫克/100毫升 |
(1)某人驾车时经交警检查每100毫升血液中酒精含量为138毫克,他属于_____驾车;
(2)乙醇(C2H5OH)俗名酒精,由____种元素组成;酒精燃烧的化学方程式________。
(3)乙醇中碳、氧两元素的质量比为:____________________。
【题目】为探究酸、碱、盐的化学性质,某兴趣小组做了如下实验。试回答下列问题:
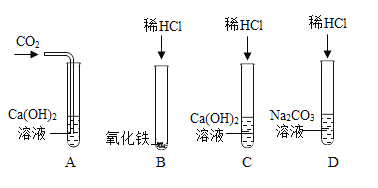
(1)试管A中的现象是__________;
(2)试管B中反应的化学方程式为__________________;
(3)甲同学把反应后C、D试管中的废液倒入一只烧杯中,观察到先有气泡产生,后有白色沉淀生成;过滤后得到白色沉淀和无色滤液。甲同学欲探究无色滤液中溶质的成分。
(提出问题)无色滤液中的溶质是什么?
(作出猜想)猜想Ⅰ:NaCl;
猜想Ⅱ:NaCl和CaCl2;
猜想Ⅲ:NaCl 和Na2CO3;
猜想Ⅳ:NaCl、CaCl2 和Na2CO3。
小明认为猜想Ⅳ一定不成立,原因是________________。
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
(1)取少量滤液于试管中,滴加少量Na2CO3溶液 | 无明显现象 | 猜想___成立 |
(2)取少量滤液于试管中,滴加少量_____ | 有气泡产生 |