题目内容
【题目】金属与人类的生产、生活密切相关,牢固掌握金属的知识非常重要。
(1)铝和铁都是我们生活中常见的金属,铝耐腐蚀性能比铁好的原因是_____。
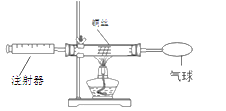
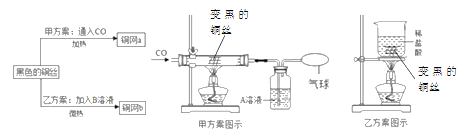
(2)如图是一氧化碳还原氧化铁的实验装置,请回答下列问题。
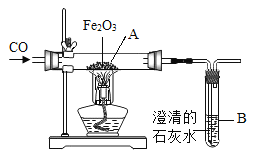
①玻璃管A中的实验现象是_____。
②实验开始时,先通入一氧化碳的原因是_____。
③从环保角度考虑,还需对以上装置进行改进,请简述改进措施_______。
(3)为了验证Fe、Cu、Ag三种金属的活动性顺序,请你写出两种可行方案所需的物质。
方案一:_______
方案二:_______
(4)若除去FeCl2溶液中杂质CuCl2,请写出有关的化学方程式。_____
(5)实验室在高温条件下,用足量一氧化碳还原10g赤铁矿,充分反应后,测得生成的纯铁的质量为5.6g。则该赤铁矿中氧化铁的质量分数是_____。
【答案】铝和氧气反应生成一层致密的氧化铝保护膜,阻止了内部的铝被氧化 红色物质变成黑色 一氧化碳气体是可燃性气体,所以在点燃前要先通入一氧化碳气体使装置中的空气排净,然后再加热,防止气体不纯,加热时发生爆炸 一氧化碳能毒不能直接排放到空气中,在装置的最右端放一燃着的酒精灯 把铁丝、银丝分别伸入硫酸铜溶液中时,铁丝表面析出红色固体,是因为铁和硫酸铜反应生成硫酸亚铁和铜,说明铁比铜活泼,银丝表面无明显现象,说明铜比银活泼,可选用Fe、CuSO4溶液、Ag 把铜丝分别伸入FeSO4溶液、AgNO3溶液中时,伸入硫酸亚铁溶液的铜丝表面无明显现象,说明铁比铜活泼,伸入硝酸银溶液中的铜丝表面析出银白色固体,说明铜比银活泼,可选用FeSO4溶液、Cu、AgNO3溶液 Fe+CuCl2=FeCl2+Cu 80%
【解析】
(1)铝耐腐蚀性能比铁好的原因是:铝和氧气反应生成一层致密的氧化铝保护膜,阻止了内部的铝被氧化;
(2)①一氧化碳和氧化铁反应生成二氧化碳和铁,现象为:红色物质变成黑色;
②由于一氧化碳气体是可燃性气体,所以在点燃前要先通入一氧化碳气体使装置中的空气排净,然后再加热,防止气体不纯,加热时发生爆炸;
③因为一氧化碳能毒不能直接排放到空气中,在装置的最右端放一燃着的酒精灯;
(3)①把铁丝、银丝分别伸入硫酸铜溶液中时,铁丝表面析出红色固体,是因为铁和硫酸铜反应生成硫酸亚铁和铜,说明铁比铜活泼,银丝表面无明显现象,说明铜比银活泼,可选用Fe、CuSO4溶液、Ag;
②把铜丝分别伸入FeSO4溶液、AgNO3溶液中时,伸入硫酸亚铁溶液的铜丝表面无明显现象,说明铁比铜活泼,伸入硝酸银溶液中的铜丝表面析出银白色固体,说明铜比银活泼,可选用FeSO4溶液、Cu、AgNO3溶液;
(4)铁和氯化铜反应生成氯化亚铁和铜,化学方程式为:Fe+CuCl2=FeCl2+Cu;
(5)设生成5.6g铁需要氧化铁的质量为x。

![]()
x=8g
该赤铁矿中氧化铁的质量分数为:
![]() =80%
=80%

【题目】下表是几种可燃物在常压时的沸点;
可燃物 | CH4 | C2H6 | C3H8 | X | C5H12 |
沸点/℃ | 164 | 88.6 | 42.1 | 0.5 | 36.1 |
(1)在C3H8中,碳元素与氢元素的质量比为_____________(最简整数比)。
(2)在C3H8中,碳元素的质量分数为_____________(计算结果精确至0.1%)。
(3)45gC2H6与_____________gC5H12所含碳元素质量相等。
(4)分析上表中可燃物分子结构上的规律,推测X的化学式为_____________。
【题目】据央视报道,有不法酒类生产企业在白酒中添加酯类物质以增强口感。下表中是机中常见的酯。
酯的名称 | 甲酸甲酯 | 甲酸乙酯 | 乙酸甲酯 | 乙酸乙酯 |
化学式 | C2H4O2 | C3H8O2 | C2H8O2 | X |
(1)比较归纳是学习化学的重要方法,上述物质的共同特点是______(写出一条即可)。
(2)甲酸甲酯(C2H4O2)中碳、氢、氧的原子个数为______。
(3)据表推测X的化学式为______。
(4)请计算乙酸甲酯(C2H8O2)中碳、氢、氧三种元素的质量之比______。
(5)试计算甲酸甲酯中碳元素的质量分数______