题目内容
【题目】根据下列实验装置图,回答有关问题。
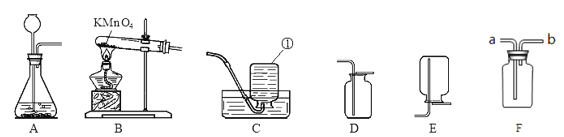
(1)图中标有①的仪器名称是______________。
(2)实验室制取氢气应选择的发生装置是__________,若要获得较纯净的氢气,应选择的收集装置是__________。为保证安全,点燃氢气前,应进行的操作是_____________。
(3)实验室利用过氧化氢溶液和二氧化锰制氧气,反应的化学方程式为__;若用B装置作制氧气的发生装置,应进行的改进是__________;反应的化学方程式为_________;若用装置F收集氧气,则气体应从导管_______(填“a”或者“b”)端通入;实验结束时应先移出导管再熄灭酒精灯,若操作顺序相反,则可能造成___________。
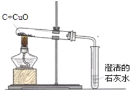
(4)排水法收集与排空气法收集二氧化碳的比较(分别用体积相同的两个集气瓶收集)
已知:CO2+H2O+CaCO3==Ca(HCO3)2,Ca(HCO3)2能溶于水。
比较项目 | 排水法 | 向上排空气法 |
收集方法可行性分析 | 因为CO2气体生成和从水面逸出的速率远大于其溶解和与水反应的速率,所以可以用排水法收集 | 因为________,所以可用向上排空气法收集 |
收集过程分析 | 集满现象:____________ | “验满”因气体无色,故集满与否较难确定,即便用燃着的木条移近容器口火焰熄灭,也难以证明空气完全排尽 |
向收集到CO2的集气瓶内倒入等体积适量澄清石灰水,并振荡 | 先浑浊后澄清所需时间较短 | 先浑浊后澄清所需时间较长 |
由上述实验可得结论 | 与排空气法相比,排水法的优点是__________ | |
【答案】集气瓶 A C 验纯 2H2O2![]() 2H2O+O2↑ 在试管口放一团棉花 2KMnO4
2H2O+O2↑ 在试管口放一团棉花 2KMnO4![]() K2MnO4+MnO2+O2↑ a 水槽中的水倒吸入试管,使试管炸裂 二氧化碳密度大于空气 集气瓶口有气泡向外冒出 收集到的二氧化碳更纯净
K2MnO4+MnO2+O2↑ a 水槽中的水倒吸入试管,使试管炸裂 二氧化碳密度大于空气 集气瓶口有气泡向外冒出 收集到的二氧化碳更纯净
【解析】
(1)图中标有①的仪器名称是集气瓶,故填集气瓶。
(2)化学上常用锌粒和稀硫酸反应制取氢气,反应是固体和液体在常温反应生成气体,发生装置应选择固液常温发生装置,故填A;
排水法收集的气体比排空气法收集的气体纯净,应选择排水法收集较纯净的氢气,故填C;
点燃可燃性气体前,为防止气体中混有氧气遇火发生爆炸,应进行的操作是检验气体的纯度,故填验纯。
(3)过氧化氢在二氧化锰作催化剂的条件下反应生成水和氧气,故反应的化学方程式写为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
加热高锰酸钾制取氧气时,应在试管口放一团棉花,防止高锰酸钾粉末进入导管,故填在试管口放一团棉花;
高锰酸钾在加热的条件下反应生成锰酸钾、二氧化锰和氧气,故反应的化学方程式写为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
用多功能瓶采用排空气法收集氧气,由于氧气的密度大于空气的密度,氧气应从长管进入瓶中,故填a;
加热高锰酸钾制取氧气,实验结束时,如果应先熄灭酒精灯再移出导管,会造成水槽中的水倒吸入试管,使试管炸裂,故填水槽中的水倒吸入试管,使试管炸裂。
(4)由于二氧化碳的密度大于空气的密度,可以选用向上排空气法收集二氧化碳,故填二氧化碳密度大于空气的密度;
用排水法收集气体集满的现象是集气瓶口有气泡向外冒出,故填集气瓶口有气泡向外冒出;
用排水法收集到的气体不含空气,气体的纯度比较高,故填收集到的二氧化碳更纯净。

【题目】某同学为了测定实验室中氯酸钾样品的纯度。取2.5克该样品与0.5克二氧化锰混合,加热一段时间后(杂质不参加反应),冷却,称量剩余物质量,重复上述操作,记录数据如下表:
加热时间 | T1 | T2 | T3 | T4 |
剩余物质量 | 2.12 | 2.08 | 2.04 | 2.04 |
①加热到T2时间后,氯酸钾是否已经反应完全?_____
②样品中氯酸钾的质量分数_______
【题目】某小组同学为探究二氧化锰对过氧化氢分解速度的影响,设计了以下实验:
(1)完善实验一、实验二:
实验步骤 | 实验现象 | 实验结论 | |
实验一 |
| 带火星的木条不复燃 | 过氧化氢分解的速率较慢 |
实验二 |
| ___________ | ________ |
(2)实验三:待实验二结束,剩余的液体化学式为_____,倒出多余液体,继续向其中加入5%的过氧化氢溶液,实验现象为____________,得出结论__________,写出此时的反应方程式__________;
(3)实验四,实验之前称量加入二氧化锰的质量为m1,待实验三结束后,取出二氧化锰,干燥后称量质量为m2,则m1_____m2(填“>”、“<”、“=”),得出结论___________,从液体中取出二氧化锰的操作名称为______;