题目内容
【题目】如图是盐酸和氢氧化钠反应过程中溶液pH变化过程图像。
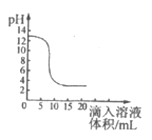
(1)根据曲线判断,该反应是将______(填“氢氧化钠溶液”或“盐酸”)滴入另一溶液中。
(2)该反应的化学方程式为______。
(3)当滴入溶液的体积为15mL时,所得溶液中的溶质为______(填化学式),此时向溶液中滴加少量碳酸钠溶液,请写出该反应的化学方程式______。
【答案】盐酸 ![]() NaCl、HCl(两种物质缺一不给分)
NaCl、HCl(两种物质缺一不给分) ![]()
【解析】
(1)氢氧化钠溶液显碱性,溶液pH>7,盐酸溶液显酸性,溶液pH<7,图像开始时溶液的pH>7,说明溶液显碱性,是氢氧化钠溶液,随着反应的不断进行,pH逐渐减小,判断该反应是将盐酸滴入到氢氧化钠溶液中;
(2)盐酸和氢氧化钠反应生成氯化钠和水,化学方程式为:NaOH+HCl=NaCl+H2O;
(3)观察图像,当滴入溶液的体积为15mL时,盐酸过量溶液显酸性,所得溶液中的溶质既有反应生成的氯化钠,也有过量的氯化氢,故填NaCl、HCl;此时向溶液中滴加少量碳酸钠溶液,碳酸钠和溶液中过量的盐酸反应生成氯化钠、水和二氧化碳,反应的方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑。

【题目】为探究某塑料的组成元素,设计了实验 I 和 II。回答下列问题:
I.制取氧气
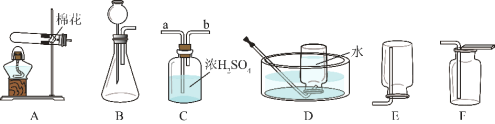
(1)若用一种暗紫色固体制取 O2,发生反应的化学方程式为_____,发生装置应选择上述装置_____(填标号)。
(2)欲制取干燥的 O2,装置合理的连接顺序为:发生装置→C→_____(填标号)。连接装置时,发生装置的出气口应与装置 C 中_____(填“a”或“b”)端相连。
II.组成探究
(3)定性检测(已知:无水 CuSO4 遇水变蓝色)
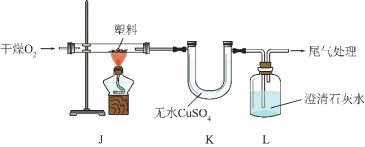
实验操作 | 实验现象 | 结论 |
连接装置,检查气密性,装入试剂并按上图进行实验。通入 O2,一段时间后,点燃 J 处酒精灯。 | 装置 K 中无水 CuSO4变①_____色 | 塑料燃烧产物中有 H2O |
装置 L 中②_____ | 塑料燃烧产物中有 CO2 |
③由上述实验可知,该塑料一定含有的元素是_____(填元素符号)。
(4)定量测定
为进一步确定组成,将 1.4g 该塑料在足量 O2 中完全燃烧,共产生了 4.4g CO2 和 1.8g H2O,依据质量守恒定律,可判断该塑料_____(填“含有”或“不含”)除上述③中结论之外的元素。