题目内容
【题目】某化学兴趣小组的同学想从含有Al2(SO4)3、CuSO4的废液中回收金属铜,设计了如图实验。
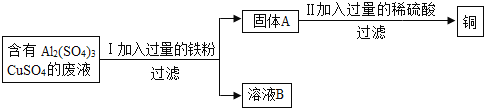
①I中有关反应的化学方程式_____
②溶液B中所含的物质除水外还含有的物质是_____
③II中加入过量的稀硫酸的目的是_____
【答案】Fe+CuSO4═FeSO4+Cu 硫酸铝、硫酸亚铁 除去铁
【解析】
① I中铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;
② 溶液B中所含的物质除水外还含有的物质是没有反应的硫酸铝和反应生成的硫酸亚铁;
③I中加入了过量的铁,固体A是铁与铜的混合物,铁与稀硫酸反应生成可溶的硫酸亚铁和氢气,铜在金属活动中排在氢之后,不能与稀硫酸反应,II中加入过量的稀硫酸的目的是除去铁。

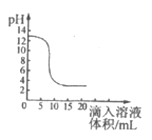
【题目】为探究盐酸的化学性质,某化学小组做了如下实验:
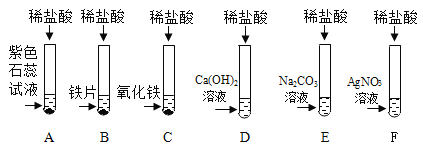
(1)上述反应中无现象的为_______(填字母序号,下同),有白色沉淀出现的是_______;B试管中所发生反应的化学方程式为_______________________________。
(2)将反应后D和E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行
探究。
(提出问题)滤液中溶质的成分是什么?
(假设与猜想)猜想一:NaCl 猜想二:NaCl和CaCl2
猜想三:NaCl、Ca(OH)2和HCl 猜想四:_____
(讨论与交流)经讨论,同学们一致认为猜想________是错误的。
(实验与结论)
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加适量碳酸钠溶液 | 无现象 | 猜想四成立 |
取少量滤液于试管中,滴加适量____ | _______ |
(拓展与迁移)稀盐酸和稀硫酸有相似的化学性质,是因为它们的溶液中都存在__________。