题目内容
【题目】阅读下面科普短文
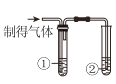
饮茶在我国具有悠久历史,茶叶中含有一类叫茶多酚的物质。茶多酚是茶叶中酚类物质及其衍生物的总称,并不是一种物质,因此常称为多酚类。茶多酚为淡黄色至茶褐色略带茶香的粉状固体或结晶,易落于水、乙醇,在空气中易氧化变色,略有吸水性。耐热性及耐酸性好,在碱性条件下易氧化褐变。从茶叶中提取茶多酚可未用下列办法。

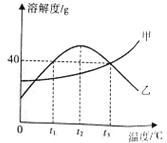
不同茶叶中茶多酚的含量不同,人们常利用茶多酚能与亚铁离子反应形成紫篮色物质,依据溶液颜色的深浅与茶多酚含量成正比的原理,测定不同种类、不同品质的茶叶中茶多酚含量。下图1和图2为不同种类、不同品质的茶叶中茶多酚含童。
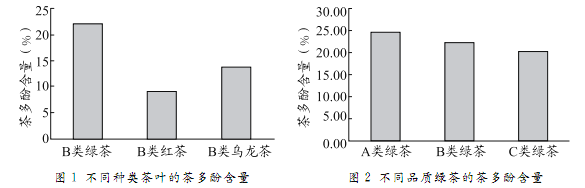
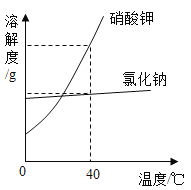
酚类物质一般都是生长在最新鲜的叶子上,茶叶越鲜嫩,茶多酚含量越高,随着茶叶生长和变老,茶多酚含童会降低。A类绿茶所选用的原料一般为一芽一叶或一芽二叶,芽的含量高,它们是茶叶中最鲜嫩的部分,生长周期短,最接近阳光能够充分与阳光进行光合作用,又具有顶端优势,叶内能合成较多的酚类物质。B类绿茶以一芽二三叶为主,C类绿茶所用的原料是生长周期更长的叶子,芽少且瘦薄。图3所示。
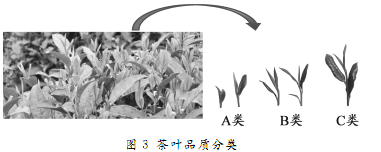
研究表明,茶多酚是茶叶中有保健功能的主要成分之一。茶多酚能够抗衰老、抗辐射、抗菌杀菌等。茶多酚对重金属具有较强的吸附作用,能与重金属形成沉淀,有利于减轻重金属叶人体产生的毒害作用。
依据文章内容回答下列问题
(1)茶多酚的物理性质有_______
(2)提取茶多酚的过程中,操作①的名称是_______
(3)由图1和图2可知,茶多酚含量最高的茶叶是____,依据文中内容解释其中茶多酚含量较高的原因是_______
(4)下列关于茶多酚的说法正确的是_______(填序号)。
A用热水泡茶会降低茶多酚含量 B茶多酚可与氧气、亚铁离子发生化学反应
C新鲜茶叶中茶多酚含量较高 D多喝绿茶有利于减少重金属的毒害作用
【答案】淡黄色至茶褐色略带茶香的粉状图体或结晶,易溶于水、乙醇 过滤 A类绿茶 茶叶鲜嫩,光合作用充分 BCD
【解析】
(1)茶多酚为淡黄色至茶褐色略带茶香的粉状图体或结晶,易溶于水、乙醇,以上性质是不需要发生化学变化就表现出来的性质是物理性质;
(2)由题意可知,提取茶多酚的过程中,操作①能将固液分开,名称是过滤;
(3)由图2和图3可知。茶多酚含量最高的茶叶是A类绿茶;依据文中内容解释其中茶多酚含量较高的原因是茶叶鲜嫩,光合作用充分。
(4)A.由题意可知,耐热性及耐酸性好,用热水泡茶不会降低茶多酚含量,故A说法不正确;
B.茶多酚可与氧气、亚铁离子发生化学反应,故B说法正确;
C.新鲜茶叶中茶多酚含量较高,故C说法正确;
D.多喝绿茶有利于减少重金属的毒害作用,故D说法正确。
故答为:(1)淡黄色至茶褐色略带茶香的粉状图体或结晶,易溶于水、乙醇;
(2)过滤;
(3)A类绿茶;茶叶鲜嫩,光合作用充分。
(4)BCD。

【题目】在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中钠在其中继续燃烧,反应后冷却,瓶底附着有黑色颗粒,同时瓶壁上粘附着白色物质.老师告诉甲同学瓶底附着黑色颗粒是碳单质,但没有告诉瓶壁上粘附着白色物质是什么,让同学们继续探究.
(进行猜想)甲同学认为:白色物质可能是Na2O或Na2CO3
乙同学认为:白色物质可能是NaOH
甲同学立刻认为乙同学的猜想是错误的,其理由是_____.
(查阅资料)氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O+H2O═2NaOH
(实验探究)甲同学对白色物质进行实验探究.
实验方案 | 实 验 操 作 | 实验现象 | 结 论 |
方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质 为Na2O |
方案2 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入适量_____溶液 | _____ | 白色物质 是Na2CO3 |
(反思评价)丙同学认为方案1得到的结论不正确,理由是_____.
(得出结论)钠在二氧化碳中燃烧的化学方程式为_____.
通过以上探究,你对燃烧和灭火有什么新的认识,请写出一点._____.
【题目】某化学兴趣小组同学用大理石和盐酸反应制取CO2,将制得的气体通入新制的饱和澄清石灰水时,发现有气泡冒出,但一段时间后仍不变浑浊。对此展开了探究活动。
(提出问题)澄清石灰水未变浑浊的原因是什么?
(猜想与假设)
I.制得气体中无CO2,II、与盐酸的浓度有关
(进行实验)
I.初步实验—实验1小组同学取等量原试剂瓶中澄清石灰水于试管内进行实验
实验操作 | 现象 | 初步结论 |
| 试管1澄清石灰水未变浑浊 试管2澄清石灰水变浑浊 | (1)可知猜想I____(填“成立”或“不成立”)。 (2)写出试管②中发生的化学反应方程式_____。 |
II.依据初步结论,深入探究;实验2
实验序号 | ① | ② | ③ | ④ | ⑤ |
大理石质量(g) | 10 | 10 | 10 | 10 | 10 |
盐酸质量分数(%) | 37.5 | 20.3 | 13.9 | 10.6 | 8.5 |
盐酸体积(mL) | 10 | 10 | 10 | 10 | 10 |
将产生的气体通入5mL新制饱和澄清石灰水中的现象 | 无 | 无 | 出现浑浊 | 出现浑浊 | 出现浑浊 |
实验3: 125 mL集气瓶中充入不同体积CO2进行实验
实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
CO2体积(mL) | 3 | 25 | 50 | 75 | 100 | 125 |
加入5ml饱和澄清石灰水振荡5次现象 | 澄清 | 变浑浊 | 变浑浊 | 变浑浊 | 变浑浊 | 变浑浊 |
振荡30次后现象 | 澄清 | 浑浊 | 浑浊 | 浑浊 | 澄清 | 澄清 |
(解释与结论)
(3)实验2的目的是_______
(4)有一定量HCl气体存在时,请解释澄清石灰水不变浑浊原因是_______
(5)由实验2,可推测质量分数为9.5%的盐酸参加反应,其可能的现象是_______
(反思与评价)
(6)由实验3可知,用澄清的石灰水检验二氧化碳时,为了得到准确的实验现象,加入二氧化碳的量不能过少也不能过多。得出此结论所依据的现象是_______
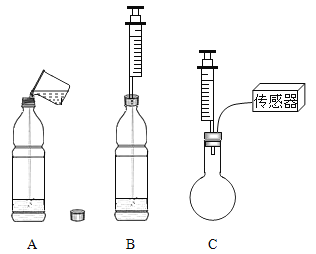
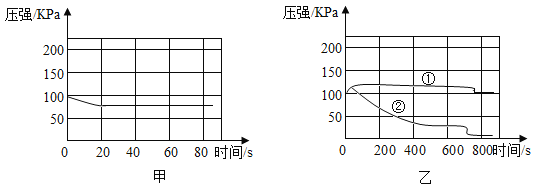
【题目】学校实验小组验证反应原理,在室温为15℃时,同学们将10g氢氧化钠固体完全溶解溶于80g水中,而后匀速的通入二氧化碳气体。同时用传感器测定溶液的pH变化,同时用数据采集器记录并绘制图像如图2所示。
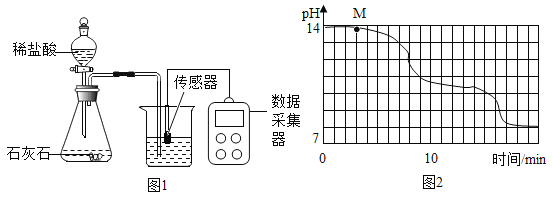
(1)图1所示实验中,用“分液漏斗”而不用“长颈漏斗”其原因是______________;
(2)通过图像分析,小苏打溶液是显________(填“酸性”、“中性”或“碱性”),图像中M点处发生的主要化学反应方程式为________________;
(3)为了确定M处溶液的成分,同学们进行如下实验:
实验步骤 | 加入试剂 | 实验现象 | 初步实验结论 |
① | 滴入________ | 溶液变红 | 有________生成 |
② | 加入________ | _______ | _______ |
(4)实验过程中,同学们发现18min后溶液的pH基本不再变化,则此时烧杯中就可观察到的现象有________。
【题目】高锰酸钾在生产、生活中有广泛的应用。实验小组同学查阅资料得知,草酸(H2C2O4)可使滴有硫酸的高锰酸钾溶液褪色,但不同条件下褪色时间不同,即反应的速率不同。小组同学进行了如下探究。
(提出问题)影响该反应反应速率的因素有哪些?
(作出猜想)影响该反应反应速率的因素有温度、催化剂、硫酸的浓度等。
(查阅资料)硫酸锰(MnSO4)可作该反应的催化剂。
(进行实验)取A、B、C、D 4支试管,每支试管中分别加入4mL 0.08% 的KMnO4 溶液、0.4 mL 的硫酸、1mL 0.09% 的 H2C2O4 溶液。

(实验记录)
序号 | 所滴硫酸浓度 | 温度 | 催化剂 | 高锰酸钾完全褪色时间 |
A | 98% | 室温 | 无 | 72s |
B | 65% | 室温 | 无 | 129s |
C | 65% | 50℃ | 无 | 16s |
D | 65% | 室温 | MnSO4 | 112s |
(解释与结论)
(1)草酸使高锰酸钾溶液褪色反应的化学方程式如下,请在横线上补全方程式。
2KMnO4 + 5H2C2O4 + 3H2SO4 == K2SO4 + 2MnSO4 + 10_______+ 8H2O
(2)4支试管中作为对照实验的是_______(填序号,下同)。
(3)设计实验A和B的目的是 ______________________________。
(4)对比实验B和C可得出的结论是_____________________________。
(5)探究催化剂对该反应反应速率影响的实验是____________________________。
(反思与交流)
(6)影响该反应反应速率的因素除温度、催化剂、硫酸的浓度外,还可能有_______。