��Ŀ����
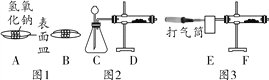
����Ŀ���������ʵ�����֮��Ĺ�ϵ��ͼ1��ʾ��
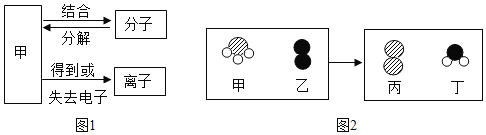
��1������_____��
��2�������������Ȼ���3�������У������ӹ��ɵ���_____��д��ѧʽ����
��3����ԭ�ӽṹʾ��ͼΪ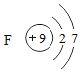 ����ԭ���ڻ�ѧ��Ӧ����_____����õ�����ʧȥ�������ӣ��ɸ�Ԫ�غͷ�Ԫ����ɵĻ���������ƵĻ�ѧʽΪ_____����Ԫ�غ���Ԫ���γɵĻ������ˮ��Һ����ᣨHF���������ڲ�����̣�����Ҫԭ����������벣������Ҫ�ɷֶ������裨SiO2��������Ӧ�������ķ��������壨SiF4����ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ_____��
����ԭ���ڻ�ѧ��Ӧ����_____����õ�����ʧȥ�������ӣ��ɸ�Ԫ�غͷ�Ԫ����ɵĻ���������ƵĻ�ѧʽΪ_____����Ԫ�غ���Ԫ���γɵĻ������ˮ��Һ����ᣨHF���������ڲ�����̣�����Ҫԭ����������벣������Ҫ�ɷֶ������裨SiO2��������Ӧ�������ķ��������壨SiF4����ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ_____��
��4��һ�������£����ҷ�Ӧ���ɱ��Ͷ����������ʾ��ɷ��ӹ��ɣ�����Ӧǰ����ʾ��ͼ��ͼ2��ʾ������˵����ȷ����_____������ĸ��ţ���
A ��Ӧǰ����4��ԭ��
B �÷�Ӧ�е�������
C ��Ӧǰ��Ԫ�ػ��ϼ۶�����
D ��ѧ�仯�з��Ӻ�ԭ�Ӿ����ٷ�
E �û�ѧ��Ӧ�У��ס������ַ��ӵĸ�������2��3
���𰸡�ԭ�� NaCl �õ� CaF2 4HF+SiO2��SiF4��+2H2O BE
��������
��1������ԭ�ӿɹ��ɷ��ӣ�ԭ��ͨ�����ӵĵ�ʧ�γ������ӣ����Լ���ԭ�ӣ�
��2���������������Ȼ���3�������У������ӹ��ɵ����Ȼ��ƣ���ѧʽ�ǣ�NaCl��
��3���ɷ�ԭ�ӽṹʾ��ͼ��֪��������������7������4����ԭ���ڻ�ѧ��Ӧ���õ�һ�����ӣ����ϼ�ӦΪ��1�ۣ���Ԫ�صĻ��ϼ�Ϊ+2�ۣ����ԣ���Ԫ���ɺͷ�Ԫ����ɵĻ���������ƵĻ�ѧʽΪCaF2����Ԫ�غ���Ԫ���γɵĻ������ˮ��Һ����ᣨHF���������ڲ�����̣�����Ҫԭ����������벣������Ҫ�ɷֶ������裨SiO2��������Ӧ�������ķ��������壨SiF4����ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ��4HF+SiO2��SiF4��+2H2O��
��4��A����ͼ��֪����Ӧǰ��һ����3��ԭ�ӣ���A����
B��������ָ��ͬ��Ԫ����ɵĴ�����÷�Ӧ�е������ɣ���B��ȷ��
C��Ԫ���ڵ����л��ϼ�Ϊ�㣬�ʷ�Ӧǰ��һ���л��ϼ۵ı仯����C����
D����ѧ�仯�з��ӿ��ٷ֣���ԭ�Ӳ����ٷ֣���D����
E����ͼ��֪�����������غ㶨�ɿ�֪Ҫ����ԭ���غ�ʱ���ס������ַ��ӵĸ�������2��3����E��ȷ���ʴ�Ϊ����1��ԭ�ӣ���2��NaCl����3���õ���CaF2��4HF+SiO2��SiF4��+2H2O����4��BE��

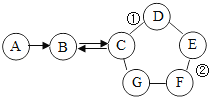
����Ŀ����һ����ɫ��ĩ��Ʒ�����к���̼���ơ��������ơ�̼��ơ���ʯ�ҡ��Ȼ��ơ�����ͭ���������е����֡���ѧ��ȤС��Ϊȷ���������Ʋ���������ʵ�顣
ʵ��һ������ͬѧ���ж���̽��
ʵ����� | ʵ������ | ʵ����ۼ����� |
��1��ȡ��������Ʒ���ձ��У�����������ˮ�ܽ⡢���� | ��ĩ�����ܽ⣬�õ���ɫ��������ɫ��Һ | ԭ��Ʒ��һ������_____�� |
��2������Һ�еμ���ɫ��̪��Һ | ��Һ��� | ��Һ�д���_____�����ʣ��������������������������� |
��3����2���еμ�����ϡ���� | _____ | ԭ��Ʒ��һ������̼���� |
ʵ���������ͬѧ���ж���̽������ͼ��
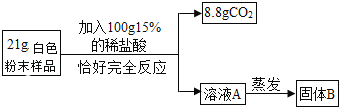
ʵ���ù���B�к�15g��Ԫ�أ��ۺϼס�������ͬѧ��ʵ����з�����
��1������ʵ����һ�������Ļ�ѧ��Ӧ��̼������ϡ����ķ�Ӧ��_____���û�ѧ����ʽ��ʾ����
��2����δ֪��ĩ����ɿ�����_____��