题目内容
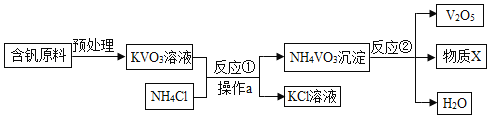
【题目】某热电厂用脱硫得到的石膏(CaSO42H2O)生产K2SO4肥料的流程如下:
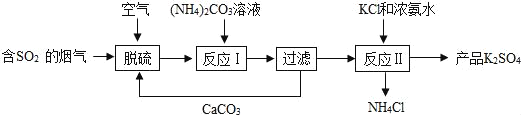
请回答下列问题:
(1)石膏中S的化合价是___.脱硫过程的化学方程式2CaCO3+2SO2+O2+4H2O=2CaSO42H2O+2___.
(2)石膏与饱和(NH4)2CO3溶液相混合,发生反应Ⅰ时需不断搅拌,其目的是___.
(3)实验室完成过滤操作所需要用到玻璃棒,玻璃棒的作用是___.
(4)(NH4)2SO4与KCl溶液需在浓氨水中发生反应Ⅱ,析出K2SO4晶体.此反应的基本类型是___.
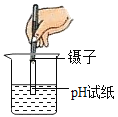
(5)该工艺可以循环利用的物质有___,副产品NH4Cl与NaOH溶液混合微热,产生的气体能使湿润的红色石蕊试纸变___色.
【答案】+6 CO2 使原料充分反应,提高原料利用率 引流 复分解 碳酸钙 蓝
【解析】
(1)在CaSO42H2O中,由于钙显+2价、氧显﹣2价、氢显+1价,所以,硫显+6价.由质量守恒定律反应前后原子的种类及数目不变可知,应填入的物质是CO2;故填:+6;CO2
(2)石膏与饱和(NH4)2CO3溶液相混合,发生反应Ⅰ时需不断搅拌,其目的是使原料充分反应,提高原料利用率;故填:使原料充分反应,提高原料利用率
(3)实验室完成过滤操作所需要的仪器有铁架台、玻璃棒以及烧杯和漏斗,玻璃棒的作用是引流;故填:引流
(4)(NH4)2SO4与KCl溶液需在浓氨水中发生反应Ⅱ,析出K2SO4晶体,生成了氯化铵,是两种化合物相互交换了成分生成了另外两种化合物,属于复分解反应;故填:复分解
(5)由反应的流程可知,该工艺可以循环利用的物质是碳酸钙,由于NH4Cl与NaOH溶液混合微热,产生了氨气,氨气的水溶液显碱性,能使湿润的红色石蕊试纸变蓝色。故填:碳酸钙;蓝

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
相关题目