题目内容
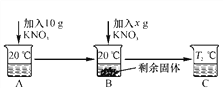
【题目】KCl与KNO3在不同温度的溶解度数据如下表。则下列说法不正确的是( )
温度/ ℃ | 20 | 30 | 40 | 50 |
KCl | 34.0 g | 37.0 g | 40.0 g | 42.6 g |
KNO3 | 31.6 g | 45.8 g | 63.9 g | 85.5 g |
A. 20 ℃时,KCl溶解度大于KNO3的溶解度
B. 两物质溶解度相等的温度在20~30 ℃之间
C. 40 ℃时,5 g KCl加10 g水可得到33.3%溶液
D. 50 ℃时,10 g KNO3中加20 g水,充分溶解,再降温到30 ℃,有KNO3固体析出
【答案】C
【解析】A、由两种物质的溶解度可知20℃时,KNO3溶解度小于KC1的溶解度,正确;B、由表格数据可知温度在20~30℃时,两物质的溶解度有相同的部分,即两物质溶解度相等的温度在20~30℃之间,正确;C、40℃时,KCl的溶解度为40g,即该温度下40g氯化钾溶解在100g水中恰好形成饱和溶液,那么10g水中最多溶解4g氯化钾,形成的溶液的溶质质量分数=![]() ×100%=28.6%,错误;D、30℃时硝酸钾的溶解度为45.8g,即该温度下45.8g硝酸钾溶解在100g水中恰好形成饱和溶液,那么20g水中最多溶解硝酸钾9.16g,即50℃时,10gKNO3中加20g水,充分溶解,再降温到30℃,有KNO3固体析出,正确。故选C。
×100%=28.6%,错误;D、30℃时硝酸钾的溶解度为45.8g,即该温度下45.8g硝酸钾溶解在100g水中恰好形成饱和溶液,那么20g水中最多溶解硝酸钾9.16g,即50℃时,10gKNO3中加20g水,充分溶解,再降温到30℃,有KNO3固体析出,正确。故选C。

【题目】以下是芳芳小朋友血液中某些元素检测结果的报告单(部分)。
序号 | 检测项目 | 结果 | 参考值 |
1 | 锌 | 7.7 | 11-22 μmol/L |
2 | 铜 | 16.9 | 14-29 μmol/L |
3 | 铁 | 17.8 | 9.0-21.5 μmol/L |
4 | 钙 | 2.0 | 2.2-2.7 μmol/L |
5 | 镁 | 0.84 | 0.8-1.2 μmol/L |
6 | 铅 | 0.28 | 0-0.48 μmol/L |
根据此份报告单并结合自己所学知识回答以下问题:
(1)芳芳缺乏的常量元素是________(填元素符号);芳芳缺乏此元素会________________;检测项目中属于有害元素的是________(填元素符号)。
(2)根据检测结果,医生建议她每天补充10 mg的锌,芳芳的爸爸给她买了下面的补锌剂:

试通过计算说明芳芳每天一共应该吃________片。
(3)芳芳的妈妈认为葡萄糖酸锌片是营养补剂,多吃几片没关系。请你评价这一观点,并说明理由。
______________________________________________
【题目】如下图(夹持仪器已略),某兴趣小组在老师指导下,探究铁与水蒸气的反应,请回答。
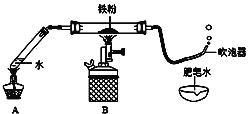
【实验初探】
(1)连接装置,并___________。
(2)装好药品。
(3)加热一段时间后,吹泡器连续吹出气泡,且气泡向上飞起,用燃着的木条靠近气泡,能产生爆鸣。
该气体燃烧的化学方程式为________。
【查阅资料】铁有三种氧化物(FeO、Fe2O3、Fe3O4)。
①它们都不溶于水,其中铁粉、Fe3O4能被磁铁吸引;②FeO接触到空气会立即由黑色变为红棕色;③三种氧化物都不与硫酸铜溶液反应,但能与酸反应生成可溶性物质。
【实验探究】实验小组同学对反应后的剩余固体进行探究。
(1)小梅发现固体为黑色,由此判断:固体中肯定不存在Fe2O3 ,理由是_______。
(2)小宇发现固体均能被磁铁吸引,大家倒出玻璃管中黑色固体,平铺于白纸上。观察现象是__________,判断黑色固体中一定没有FeO。
讨论:铁与水蒸气反应生成的固体是“铁的一种氧化物”,玻璃管内的黑色固体中还可能含有“过量的铁”。
【提出猜想】玻璃管中黑色固体成分有什么?
猜想Ⅰ:Fe; 猜想Ⅱ:Fe3O4; 猜想Ⅲ:______________
实验步骤 | 实验现象 | 实验结论 |
取上述固体少许,加入足量 _________________ | 出现红色固体,且有黑色固体残留 | 黑色固体中一定含有 ________________ |
【结论反思】(1)铁与水蒸气发生置换反应,反应的方程式是________________。
(2)出现红色固体的化学方程式是_______,加入的溶液必须足量的原因是______________。