题目内容
【题目】已知20 ℃时,在100 g水中达到饱和所能溶解的KNO3的最大量是31.6 g。向50 mL水(密度是1 g/mL)中溶解一定量KNO3固体如下。请回答:
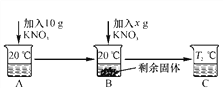
(1)A、B、C中一定是饱和溶液的是________(填字母)。
(2)当x=________g时,B中恰好没有固体剩余。
(3)硝酸钾晶体从溶液中析出常用______________的方法。
【答案】 B 5.8 降温结晶(或冷却热饱和溶液)
【解析】(1)20℃时硝酸钾的溶解度是31.6g,50mL水就是50g水,能溶解硝酸钾的质量最多是15.8g,故加入10g硝酸钾形成的A溶液是不饱和溶液,继续加入Xg硝酸钾,形成的溶液B有固体剩余,故B是饱和溶液,温度升高到T℃形成的溶液C,固体无剩余,因为不知道具体的温度,故硝酸钾可以是恰好溶解形成饱和溶液,也可能是溶解后形成不饱和溶液;(2) 20℃硝酸钾的溶解度是31.6g,50g水中最多溶解15.8g,已经加入了10g,所以还需加入硝酸钾质量为:15.8g-10g=5.8g;(3)硝酸钾的溶解度随温度升高而增大,且变化较大,所以要得到其晶体可采取降温结晶或冷却热饱和溶液的方法。

 名校课堂系列答案
名校课堂系列答案【题目】硅钢是制变压器、充电器的核心材料,其主要成分是Fe和Si。某同学用硅钢样品进行如下实验:取6.60 g硅钢样品,将60.00 g稀硫酸分6次加入样品中(其中稀硫酸与硅及其他杂质不反应)。实验测得相关数据如下:
稀硫酸的用量 | 剩余固体的质量 |
第1次加入10.00 g | W g |
第2次加入10.00 g | 4.36 g |
第3次加入10.00 g | 3.24 g |
第4次加入10.00 g | 2.12 g |
第5次加入10.00 g | 1.00 g |
第6次加入10.00 g | 1.00 g |
(1)根据表中数据,稀硫酸加入到第________次,铁恰好反应完全。
(2)表中W=________g。
(3)计算该稀硫酸溶质的质量分数是__________(写出计算过程)。