题目内容
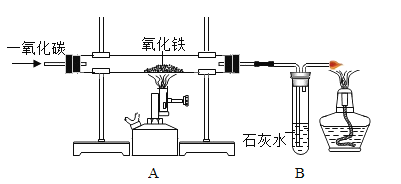
【题目】某化学兴趣小组用实验室常用药品(或溶液)对“NaOH溶液与稀盐酸是否恰好完全反应”进行探究。
(知识卡片):氯化钠溶液显中性。氯化铜易溶于水。
(实验探究):
(1)方案I:某同学先向试管中加入约2mLNaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。
①从微观的角度分析,该反应的实质是_______________。
②在滴入稀盐酸的过程中,若观察到有少量气泡出现,分析产生气泡的可能原因是NaOH变质,请写出变质的反应方程式_________。
(2)方案Ⅱ:
实验步骤 | 实验现象 | 结论 |
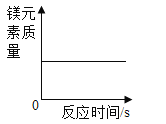
取2mLNaOH溶液于试管中,滴入一定量的稀盐酸,振荡后加入镁条 | 若________ | 稀盐酸过量 |
若没有明显现象 | NaOH 溶液与稀盐酸恰好完全反应 |
(实验反思):
(3)另有同学提出方案Ⅱ不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是:_________。
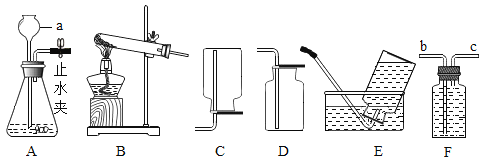
(4)除以上方案外,下列哪些物质单独使用,也能证明“NaOH溶液与稀盐酸是否恰好完全反应”__________。(填序号)
A 铜片 B pH试纸 C 氧化铜 D 紫色石蕊试液
【答案】氢离子和氢氧根离子结合成水 ![]() 有气泡产生 氢氧化钠有可能有剩余,不是恰好完全反应 BD
有气泡产生 氢氧化钠有可能有剩余,不是恰好完全反应 BD
【解析】
氢氧化钠和稀盐酸反应生成氯化钠和水,二氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳。
(1)①氢氧化钠和稀盐酸反应生成氯化钠和水,从微观的角度分析,该反应的实质是氢离子和氢氧根离子结合成水。
②二氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,故变质的反应方程式为![]() 。
。
(2)稀盐酸和氢氧化钠反应生成氯化钠和水,镁和稀盐酸反应生成氯化镁和氢气。
实验步骤 | 实验现象 | 结论 |
取2mLNaOH溶液于试管中,滴入一定量的稀盐酸,振荡后加入镁条 | 若有气泡产生 | 稀盐酸过量 |
若没有明显现象 | NaOH 溶液与稀盐酸恰好完全反应 |
[实验反思]
(3)氢氧化钠和镁不反应,和稀盐酸反应没有明显现象,方案Ⅱ不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是氢氧化钠有可能有剩余,不是恰好完全反应。
(4)氢氧化钠溶液显碱性,能使紫色石蕊试液变蓝,氢氧化钠和稀盐酸反应生成氯化钠和水,稀盐酸显酸性,能使紫色石蕊试液变红,氯化钠溶液显中性,不能使紫色石蕊试液变色,取少量反应后的溶液于试管中并滴加紫色石蕊试液,若紫色石蕊试液不变色,说明氢氧化钠溶液与稀盐酸恰好完全反应,故选BD。

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案【题目】在某密闭容器中,通过电火花点燃下列物质发生反应,它们的做观示意图和反应前后的各物质的质量如下表所示。
物质序号 | 甲 | 乙 | 丙 | 丁 |
微观示意图 |
|
|
|
|
反应前质量/g | 68 | 100 | 0 | 10 |
反应后质量/g | x | 4 | y | z |

(1)甲、乙、丙、丁四种物质中属于氧化物的是_____(填物质序号);
(2)已知该反应中有两种反应物和两种生成物,该反应的化学方程式为______。
(3)在计算x、y、z的过程中,某同学得出了以下等式,其中错误的是_____(填字母序号)。
A x+4=y+z
B x+y+z=174
C (68-x):z=17:9
D 32(z-10)=9y
【题目】根据题意填空。
(1)用化学符号表示下列图片中信息,其中“![]() ”表示氢原子,“
”表示氢原子,“![]() ”表示氧原子。
”表示氧原子。
图片 |
|
|
符号 | _____ | _____ |
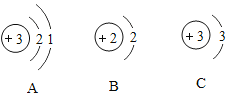
(2)现已探明月球上含有丰富的核能原料He-3(3表示相对原子质量)。氦元素的原子结构示意图为_____(填字母编号)。
(3)氯化钠是由_____(填微粒符)构成的。
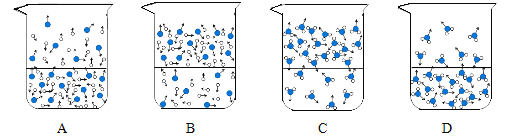
(4)保持水的化学性质的是_____(填化学符号),下列图示能反映水在空气中放置时发生变化的微观示意图是_____(填字母序号)。(图中“![]() ”表示氧原子,“
”表示氧原子,“![]() ”表示氢原子)
”表示氢原子)