题目内容
【题目】分析下列化学反应,有关说法正确的是
反应①: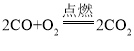
反应②: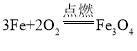
反应③: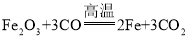
A.上述反应的生成物都是氧化物
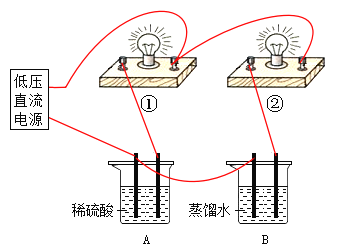
B.在实验室中进行上述反应,反应现象均相同
C.Fe2O3、Fe3O4中铁、氧元素的质量比不同
D.CO→CO2的转化只能通过反应①、③实现
【答案】C
【解析】
A、反应①、反应②中的生成物CO2、Fe3O4都是氧化物,反应③中的生成物CO2是氧化物,生成物Fe是单质,不是氧化物,选项A不正确;
B、反应①的现象是:发出蓝色火焰,放出热量,将蘸有澄清石灰水的烧杯罩在火焰上方,石灰水变浑浊;反应②的现象是:剧烈燃烧,火星四射,生成一种黑色固体,同时放出大量的热;反应③的现象是:红棕色固体逐渐变成黑色,生成的气体通入澄清石灰水,石灰水变浑浊。因此在实验室中进行上述反应,反应现象不相同,选项B不正确;
C、Fe2O3中铁、氧元素的质量比为:(56×2)∶(16×3)=7∶3;Fe3O4中铁、氧元素的质量比为:(56×3)∶(16×4)=21∶8。根据计算Fe2O3、Fe3O4中铁、氧元素的质量比不同,选项C正确;
D、CO→CO2的转化除了通过反应①、③实现,还可以通过一氧化碳和氧化铜等物质反应实现,选项D不正确。故选C。

【题目】黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品。为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
样品 | 第1份 | 第2份 | 第3份 | 第4份 | 第5份 |
取样品质量(g) | 40.0 | 40.0 | 40.0 | 40.0 | 40.0 |
取稀硫酸质量(g) | 30.0 | 60.0 | 90.0 | 120.0 | 150.0 |
产生气体质量(g) | 0.3 | 0.6 | 0.9 | 1.0 | 1.0 |
按要求回答下列问题:
(1)根据实验数据分析,从第___份开始,金属已经反应完全了。
(2)列式计算该黄铜样品中金属锌的质量分数___。(要求写出计算过程)

(3)在给出的坐标纸上,画出40.0g样品中加稀硫酸的质量与产生气体质量的关系曲线___。