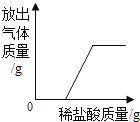
题目内容
【题目】根据下图所示的信息解答相关问题:
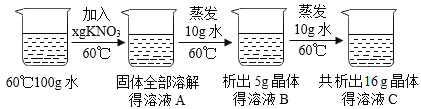
(1)溶液A一定是_______________(填“饱和”或“不饱和”)溶液。
(2)溶液B中溶剂与溶质的质量比为____________________。
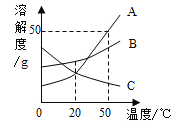
(3)如图为KNO3的溶解度曲线图,图上a点纵坐标的值为___________________。若甲物质的溶解度随温度变化的趋势与KNO3相同,则将20℃时接近饱和的甲溶液变成饱和溶液,能达到目的的是_________(填字母)。
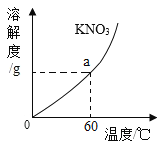
A 升温
B 降温
C 加溶质甲
D 加水
【答案】不饱和 10∶11 110 BC
【解析】
(1) 60℃时溶液A蒸发10g水,析出5g晶体,得到的溶液B是60℃时的饱和溶液,而60℃时溶液B蒸发10g水,连同第一次蒸发共析出16g晶体,即60℃时溶液B蒸发10g水,析出晶体11g,因此60℃时溶液A一定是不饱和溶液。
(2)溶液B是60℃时KNO3的饱和溶液。因为60℃时溶液B蒸发10g水,析出晶体11g,饱和溶液恒温蒸发时,析出晶体的质量和蒸发溶剂的质量之比与原饱和溶液中溶质和溶剂的质量比相同,所以溶液B中溶剂与溶质的质量比为:10g∶11g=10∶11。
(3)题中硝酸钾溶解度曲线上a点横坐标是60℃,纵坐标表示的是60℃时硝酸钾的溶解度,而题中图示溶液B是60℃时KNO3的饱和溶液, 60℃时溶液B蒸发10g水,析出晶体11g,根据溶解度的含义可以推算出60℃时硝酸钾的溶解度为110g,因此溶解度曲线图上a点纵坐标的值为110。若甲物质的溶解度随温度变化的趋势与KNO3相同,则甲物质的溶解度随温度升高而增大,随温度的降低而减小,则将20℃时接近饱和的甲溶液变成饱和溶液,可以采用的方法有:加溶质甲;降温。如果将20℃时接近饱和的甲溶液升温或加水,溶液不可能变成20℃时的饱和溶液。因此能达到目的的是:BC。

【题目】实验室用锌粒和足量的稀硫酸反应,制取氢气并还原4.0g氧化铜,实验装置如下(装置气密性良好,夹持仪器省略)。
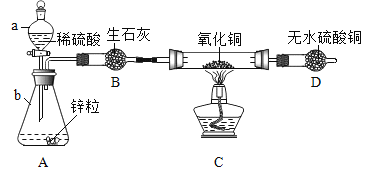
(1)仪器a的名称_______,仪器 b的名称__________。
(2) 锥形瓶中反应的化学方程式是__________,生石灰的作用是_________。
(3)要通入氢气一段时间后才能点燃酒精灯,目的是________,玻璃管中反应的化学方程式是________。
(4)为确定实验结束后氧化铜是否已基本消耗完,请设完成下表中两种不同的方案。
操作 | 判断依据 | 结论 | |
方案一 | 玻璃管中固体取样,加稀盐酸 | 现象:_______ | CuO已消耗完 |
方案二 | 称量玻璃管中残留固体质量 | 固体质量为____g |