题目内容
【题目】A﹣G是初中常见的物质.其中E为黑色固体.如图为这些物质的转化关系图,其中部分生成物和反应条件已省略.
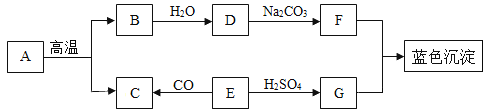
(1)写出物质E的化学式:_____.
(2)化学反应常伴有能量变化.B与水反应时会_____(“吸收”或“放出”)热量.
(3)写出D→F的化学方程式_____.
(4)可用Cu、O2和H2SO4作原料制得CuSO4,反应的过程是:_____(用文字表述).
【答案】CuO 放出 Ca(OH)2+Na2CO3═CaCO3↓+2NaOH 铜在空气加热生成氧化铜,氧化铜与稀硫酸反应生成硫酸铜和水
【解析】
A﹣G是初中常见的物质,其中E为黑色固体,A高温分解生成B和C,结合碳酸钙高温分解生成氧化钙和二氧化碳,氧化钙与水反应生成氢氧化钙,氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠;氧化铜是一种黑色粉末,可以与一氧化碳反应生成二氧化碳和铜,氧化铜还可以与硫酸反应生成硫酸铜和水,氢氧化钠与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠;则A﹣G分别是碳酸钙、氧化钙、二氧化碳、氢氧化钙、氧化铜、氢氧化钠、硫酸铜。
(1)由分析可知:物质E的化学式为:CuO;
(2)B与水反应,即氧化钙与水反应生成氢氧化钙,该反应放出大量的热;
(3)D→F,即氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(4)可用Cu、O2和H2SO4作原料制得CuSO4,铜在空气加热生成氧化铜,氧化铜与稀硫酸反应生成硫酸铜和水。

 互动英语系列答案
互动英语系列答案【题目】某兴趣小组在相同条件下,将10.00g下列物质分别置于相同规格的烧杯,并敞口存放于空气中,烧杯中所有物质的质量随时间变化如下表,回答下列问题。
时间 | 质量/g | |||||
水 | 氯化钠溶液 | 盐酸 | 浓硫酸 | 氢氧化钠浓溶液 | 氯化钙溶液 | |
1天 | 8.16 | 8.62 | 8.64 | 11.18 | 9.38 | 10.25 |
2天 | 5.76 | 6.40 | 6.69 | 12.55 | 8.47 | 10.33 |
(1)图中能反映水在空气中放置时,发生变化的微观示意图是____(填标号)。
A  B
B  C
C 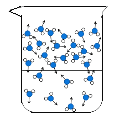 D
D 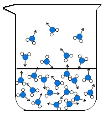
(2)为研制一种安全、环保的除湿剂,可选择上表中的____(填溶质的化学式)。
(3)为确认放置2天的盐酸浓度的变化,作如下的探究:取放置前后的盐酸分别滴入____溶液,再滴加_____相同的NaOH溶液,边滴加边振荡,当溶液颜色恰好由无色变为红色时,对比试管中溶液体积(如图所示),说明放置后盐酸溶质质量分数变____(填“大”或“小”)。

(4)氯化钠溶液放置2天后析出0.60g固体,则原氯化钠溶液是____(填“饱和溶液”或“不饱和溶液”)。(已知该温度下氯化钠的溶解度为36.0g)