题目内容
【题目】归纳总结是学习化学的重要方法,小明同学用图l总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应,图1性质②中的酸性氧化物属于非金属氧化物)。
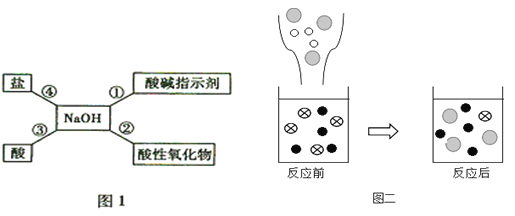
(1)验证性质①,小明将石蕊溶液滴入氢氧化钠溶液中,现象是_____;
(2)Ⅰ.为验证性质②,选取能与氢氧化钠溶液反应的物质是_____(填选项)
A CO B SO3 C HNO3 D CO2
Ⅱ.写出上述反应的化学方程式_____(只写一个):
(3)为验证性质③,小明往氢氧化钠溶液中滴加稀盐酸。
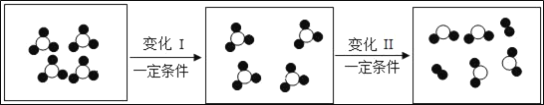
①图二表示该反应前后溶液中存在的主要离子,请写出下列图形代表的离子(填离子符号):![]() _____,
_____,![]() _____;
_____;
②从图二中可以看出,反应后的溶液pH_____7(填“>”、“<”或“=”)。
【答案】紫色石蕊溶液变蓝 .BD 2NaOH+SO3=Na2SO4+H2O或2NaOH+CO2=Na2CO3+H2O Na+ Cl- >
【解析】
(1)紫色石蕊试液遇碱性溶液变蓝,验证性质①,小明将石蕊溶液滴入氢氧化钠溶液中,现象是紫色石蕊溶液变蓝;
(2)酸性氧化物是指溶于水后能与水反应生成酸的氧化物。 CO是氧化物,但不与水反应; SO3 是氧化物且能和水反应生成硫酸; HNO3 本身是酸,不是氧化物; CO2是氧化物,能与水反应生成碳酸,为验证性质②,选取能与氢氧化钠溶液反应的物质是三氧化硫和二氧化碳,故选BD;
Ⅱ.三氧化硫和氢氧化钠反应生成硫酸钠和水,反应的化学方程式:2NaOH+SO3=Na2SO4+H2O;二氧化碳和氢氧化钠反应生成碳酸钠和水,反应方程式为:2NaOH+CO2=Na2CO3+H2O;
(3)①往氢氧化钠溶液中滴加稀盐酸,盐酸和氢氧化钠反应生成氯化钠和水,反应的实质是氢离子和氢氧根离子生成水分子,图二表示该反应前后溶液中存在的主要离子,则下列图形代表的离子(填离子符号):![]() : Na+,
: Na+,![]() :Cl- ;
:Cl- ;
②从图二中可以看出,反应后氢氧根离子有剩余,溶液呈碱性,pH>7。

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案【题目】下列实验设计不能达到其对应实验目的的是( )
选项 | 实验 | 现象 | 结论 |
A |
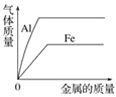
| 铁片表面有少量气泡,锌丝表面有较多气泡 | 说明铁与锌的活泼性 Fe<Zn |
B |
| 硫磺在空气中燃烧发出微弱的淡蓝色火焰,在氧气中发出明亮的蓝紫色火焰 | 说明硫磺在氧气中燃烧更旺盛 |
C |
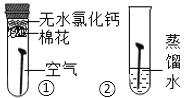
| ①试管中没有明显现象 ②试管中铁钉生锈 | 说明铁生锈需要水 |
D |
| 试管中白磷燃烧,热水中白磷不燃烧 | 说明燃烧需要氧气 |
A. AB. BC. CD. D
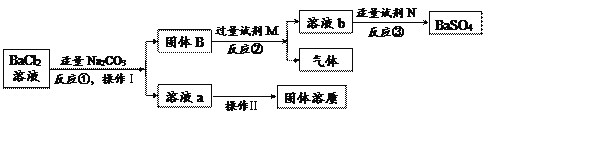
【题目】某化学兴趣小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后瓶中残留废液进行探究。

(提出问题)废液中所含溶质是什么?
(猜想与假设)
猜想1:废液中的溶质是NaCl、Na2CO3和HCl
猜想2:废液中的溶质只有NaCl
猜想3:废液中的溶质是NaCl、HCl
猜想4:废液中的溶质是______。
(讨论与交流)
小明认为猜想I无需验证就知道是错误的,他的理由是_____(请用化学方程式说明)。
(实验与结论)
(1)小亮同学为验证猜想3,取少量废液装入试管中,然后滴入酚酞溶液,发现溶液不变色,于是小亮认为猜想3正确。你认为他的结论____(填“正确”或“错误”),理由是______________。
请你另设计实验方案验证猜想3:
实验步骤 | 实验现象 | 实验结论 |
__________________ | __________________ | 猜想3正确 |
(2)验证猜想4,可选择的试剂有____________。
A.酚酞溶液B.氢氧化钾溶液C.稀硫酸D.氯化钡溶液
(拓展与应用)若废液中的溶质是NaCl和HCl,根据盐酸的性质,无需另加试剂,只要对废液进行____操作,即可从废液中得到NaCl固体。