题目内容
【题目】下列实验方案设计能达到实验目的是( )
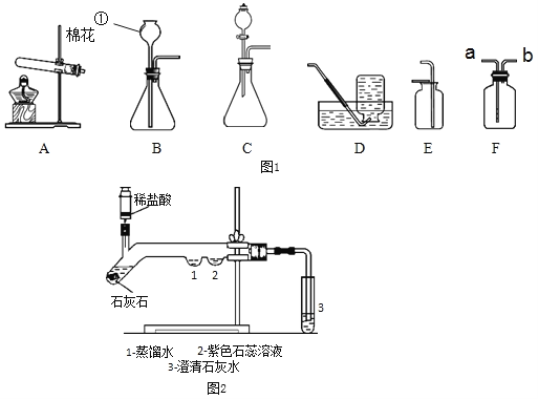
A. 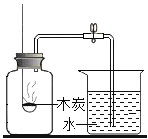 测定空气中氧气的含量
测定空气中氧气的含量
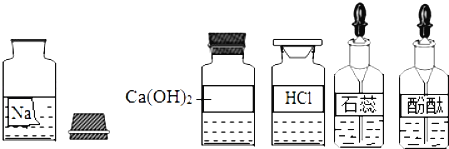
B. 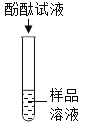 检验NaOH溶液 是否变质
检验NaOH溶液 是否变质
C. 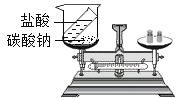 验证质量守恒定律
验证质量守恒定律
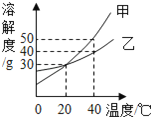
D. 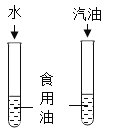 探究影响物质溶解性的因素
探究影响物质溶解性的因素
【答案】D
【解析】
A、木炭在空气中燃烧生成二氧化碳气体,虽除去氧气,而增加了新的气体,没有形成压强差,不能用来测定空气中氧气含量,故选项实验方案设计不能达到实验目的。
B、变质后的氢氧化钠溶液中含有碳酸钠,氢氧化钠和碳酸钠溶液均显碱性,均能使无色酚酞溶液变红色,不能检验NaOH溶液是否变质,故选项实验方案设计不能达到实验目的。
C、碳酸钠与稀盐酸反应生成二氧化碳气体,反应后二氧化碳气体逸出,不能用于验证质量守恒定律,故选项实验方案设计不能达到实验目的。
D、食用油难溶于水,易溶于汽油,说明同一种溶质在不同的溶剂中溶解性不同,可用于探究影响物质溶解性的因素,故选项实验方案设计能达到实验目的。
故选:D。

 智能训练练测考系列答案
智能训练练测考系列答案【题目】根据下列实验装置图,回答问题
发生装置 | 收集装置 | 洗气装置 |
|
|
|
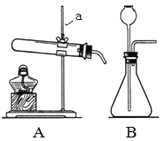
(1)写出图中仪器a的名称:___________。
(2)实验室用加热高锰酸钾制取氧气的化学方程式为___________。
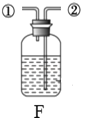
(3)实验室用石灰石和稀盐酸反应制取二氧化碳的化学方程式为___________,该反应生成的二氧化碳中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置除去氯化氢气体,则该混合气体应从F装置的___________口(填“①”或“②”)通入。
通常用澄清石灰水来检验二氧化碳,反应的化学方程式为___________。
(4)实验室需少量甲烷气,可用加热无水醋酸钠与碱石灰的固体混合物制得。制甲烷气的发生装置应选用___________(填字母)装置;收集甲烷气可选用C或E装置,由此推断甲烷气具有的物理性质是:___________。
【题目】某化学小组从理论上初步探究“已知质量比的硝酸钾和氯化钠的混合物中提纯硝酸钾”。
(分析提纯方法)
硝酸钾和氯化钠在不同温度时的溶解度
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
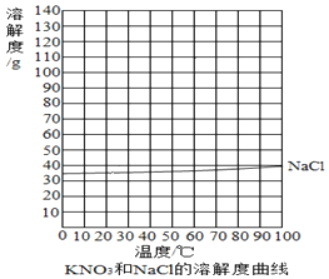
(1)20℃时,NaCl的溶解度为_____。 将20g NaCl加入50g水中配制成_____g NaCl溶液。
(2)根据表中数据,绘制KNO3的溶解度曲线_____。
(3)根据KNO3的溶解度曲线,预测KNO3在70℃时的溶解度约为_____g。
(设计提纯步骤)
①选取样品(85gKNO3和5gNaCl的混合物)
②配制80℃时KNO3的饱和溶液(加水约50mL,水的密度约为1gmL﹣1)
③降温至20℃
④得到晶体
(设计提纯方案)
(4)为了证明 ④中得到的晶体为纯净的KNO3,该小组同学结合已有知识,从理论上初步设计了以下方案;(不考虑不同溶质对溶解度的相互影响及实验过程中水和固体的损失等影响因素)
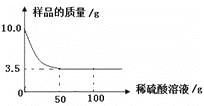
方案一 通过化学实验进行检验,取少量④中得到的晶体于试管中,加水配成溶液,滴加_____,观察实验现象没有_____产生,则不含NaCl。
方案二 计算析出KNO3晶体的质量约为_____g(精确到整数)与④中得到晶体的质量进行比较,若相等,则不含NaCl。