��Ŀ����
����Ŀ��ij��ѧ��ȤС����������װ��̽���������ȡ�����ʡ�������ͼ1�ش��й����⣺
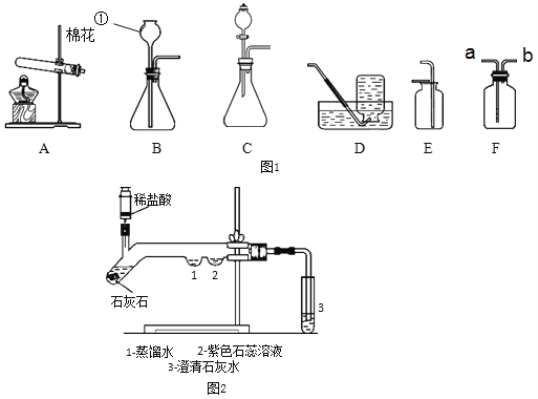
��1��д��װ��ͼ�б�����������ƣ���_____��
��2��д��ʵ������Aװ����ȡ�����Ļ�ѧ����ʽ��_____��
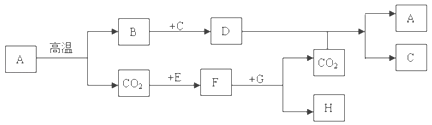
��3����Eװ�ÿ����ռ�O2��CO2��H2�е�_____������F װ���ռ�H2������Ӧ��_____����ܿ���ĸ��ͨ�롣
��4��ijͬѧ�ù���������Һ�Ͷ���������ȡO2��Ϊ�˽Ϻõؿ��Ʒ�Ӧ���ʣ���ѡ�õķ���װ����_____������ţ���
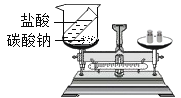
��5��Ϊ��̽��������̼�����ʣ�ijͬѧ�������ͼ2��ʾ��ʵ�飺
��ʯ��ʯ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ��_____��
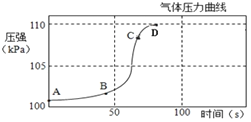
����ע����ע��ϡ���ᣬһ��ʱ��ɹ۲쵽1��2 ��������һ�������Ե�����������ʵ�������ǣ�_____��
�����ij���ʯ��ˮ����ǣ���Ӧ�Ļ�ѧ����ʽΪ��_____��
��6���������������ʵ�飺
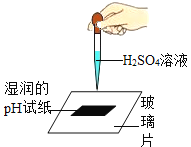
��Ũ������������Ի�����ǿ�ҵĸ�ʴ�ԣ�մ��Ƥ���ϣ�Ӧ�����ô���ˮ��ϴ��Ȼ����Ϳ��3%��5%��_____��Һ��
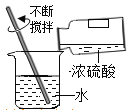
��Ũ����Ҳ������ˮ�ԣ�Ũ���᳨�ڷ���һ��ʱ���Ũ�������������������_____�����������������������������С������
�����⣬Ũ����Ҳ��������ǿ�����ԣ����������������巢����Ӧ���ɵ���ɫ�ķǽ������嵥�����д̼�����ζ����̬��������������ں�������Һ̬������÷�Ӧ�Ļ�ѧ����ʽΪ��_____��
�����Ũ������٢ڢ����ʿ�֪��������������Ũ����������_____������ţ��ɶ�ѡ����
A ������̼ B ���� C ���� D ����
���𰸡�����©�� 2KMnO4![]() K2MnO4+MnO2+O2�� O2��CO2 b C CaCO3+2HCl�TCaCl2+H2O+CO2�� 2����ɫʯ����Һ��ɺ�ɫ CO2+Ca��OH��2��CaCO3��+H2O ̼������ ��С H2SO4+H2S��S��+SO2+2H2O AD
K2MnO4+MnO2+O2�� O2��CO2 b C CaCO3+2HCl�TCaCl2+H2O+CO2�� 2����ɫʯ����Һ��ɺ�ɫ CO2+Ca��OH��2��CaCO3��+H2O ̼������ ��С H2SO4+H2S��S��+SO2+2H2O AD
��������
��1����ͼ��֪�������dz���©����
��2��װ��A�����ڹ��������ȡ���壬��Ϊ�Թܿڴ���һ�����������Ǽ��ȸ��������������ͬʱ��������غͶ������̣���Ӧ�Ļ�ѧ����ʽΪ��2KMnO4![]() K2MnO4+MnO2+O2����
K2MnO4+MnO2+O2����
��3��װ��EΪ�����ſ��������������ռ��ܶȱȿ���������壬��O2��CO2���������ܶȱȿ���С����װ��F���ռ�����ʱ�������Ӷ̹ܽ��룻
��4������װ����C�еķ�Һ©�����Կ��Ʒ�Ӧ�����ʣ�ӦѡC��
��5����ʵ������ȡCO2�����ڳ����£���̼��ƺ����ụ�ཻ���ɷ������Ȼ��ƺ�ˮ�Ͷ�����̼����ѧ����ʽΪCaCO3+2HCl�TCaCl2+H2O+CO2����
��ͼ2����ע����ע��ϡ���ᣬһ��ʱ�������̼��ˮ��Ӧ����̼�ᣬ̼����ʹ��ɫ��ʯ����Һ���ɫ�����Կɹ۲쵽��������2����ɫʯ����Һ��ɺ�ɫ��
�۴�������̼���������Ʒ�Ӧ����̼��Ƴ�����ˮ��������Ӧ�Ļ�ѧ����ʽΪCO2+Ca��OH��2��CaCO3��+H2O��
��6����Ũ������������Ի����и�ʴ�ԣ�մ��Ƥ���ϣ����������ô���ˮ��ϴ����Ϳ��3%��5%��̼��������Һ��
��Ũ����Ҳ������ˮ�ԣ���Ũ����ƿ�ǣ�Ũ��������������������С��
��Ũ�������������巢����Ӧ���ɵ���ɫ�ķǽ������嵥�����������ˮ����Ӧ�Ļ�ѧ����ʽΪ��H2SO4+H2S��S��+SO2+2H2O��
����Ϊ�������������������Ũ���ᷴӦ�����Կ���Ũ���������ǣ�������̼��������