题目内容
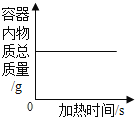
【题目】t℃时,某物质在不同质量的水中恰好达到饱和状态时所溶解的质量关系如图所示,下列说法正确的是
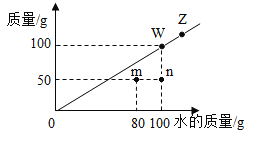
A.t℃时该物质的溶解度为50g
B.点Z→W移动的一种方法是恒温蒸发一定量的水并过滤
C.将m点的溶液变为饱和溶液的一种方法是加入20g溶质
D.图中4个点的溶液中溶质质量分数关系是:n<m<w<z
【答案】B
【解析】
A、根据溶解度的涵义,溶解度的标准是在一定温度下,在100克水最多能溶解某物质的质量的,所以t℃时该物质的溶解度应该为100g,不符合题意;
B、点Z→W移动的是温度不变,溶质质量减少,溶剂减少,方法是恒温蒸发一定量的水并过滤,符合题意;
C、t℃时该物质的溶解度应该为100g,m点的溶液中溶质是50g,水是80g,在该温度下,要使80g水变为饱和溶液需要溶质质量为![]() ,需要加入溶质的质量为80g-50g=30g,不符合题意;
,需要加入溶质的质量为80g-50g=30g,不符合题意;
D、Z点和W点是同一温度的饱和溶液,Z点和W点的溶液的溶质质量分数相等,而n点和m点在曲线外,为该温度下的不饱和溶液,所以Z点和W点的溶液的溶质质量分数大于n点和m点的溶液的溶质质量分数。而n点和m点溶液中溶质的质量相等,n点的溶剂质量大于m点的溶剂的质量,所以n点的溶液的溶质质量分数小于m点的溶液的溶质质量分数,则4个点的溶液中溶质质量分数关系是:w=z >m>n,不符合题意。故选B。

 手拉手全优练考卷系列答案
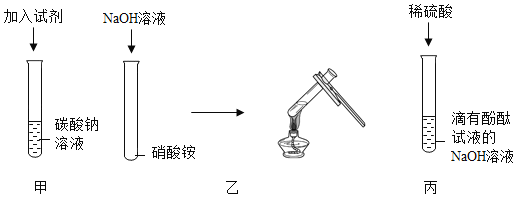
手拉手全优练考卷系列答案【题目】根据大量的实验总结,得出酸碱盐之间相互发生复分解反应的条件是生成物中有沉淀、气体或水。实验回顾如图:
请回答
(1)甲实验有沉淀生成:加入的试剂是_____;
(2)乙实验有气体生成:化学方程式_____,检验气体的方法为_____;
(3)丙实验有水生成:氢氧化钠溶液中加入酚酞的作用是_____;
(4)依据复分解反应的条件可判断硫酸和氯化镁溶液不能发生反应。若想确认两种物质没有发生复分解反应,需要检验溶液中存在_____(写微粒符号)。
提出新问题:我们已经知道能发生复分解反应的两种盐通常是可溶的。有没有某些可溶性盐和难溶性盐能发生复分解反应?
查阅资料:
难溶性盐 | AgI | AgCl |
20℃时在水中的溶解度 | 3×107g | 1.5×104g |
颜色 | 黄 | 白 |
(5)实验取证:取少量硝酸银溶液于试管中,滴加过量的氯化钠溶液,有白色沉淀产生,继续加入少量KI溶液,白色沉淀转化为黄色沉淀,加入少量KI溶液后发生反应的化学方程式_____;
(6)结论某些可溶性盐和难溶性盐之间能发生复分解反应。从微观角度分析原因:反应朝着溶液中离子浓度(单位体积溶液中离子数目的多少)_____(填“减少”或“增大”)的方向进行。
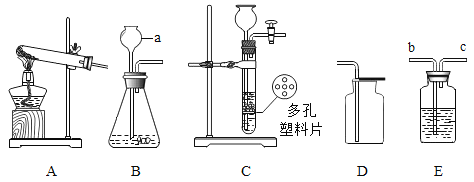
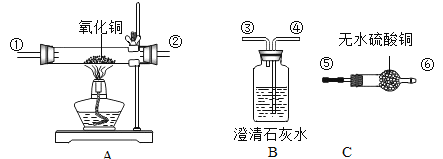
【题目】实验室用锌粒和足量的稀硫酸反应,制取氢气并还原4.0g氧化铜,实验装置如下(装置气密性良好,夹持仪器省略)。
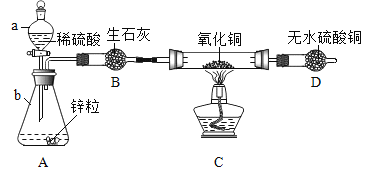
(1)仪器a的名称_______,仪器 b的名称__________。
(2) 锥形瓶中反应的化学方程式是__________,生石灰的作用是_________。
(3)要通入氢气一段时间后才能点燃酒精灯,目的是________,玻璃管中反应的化学方程式是________。
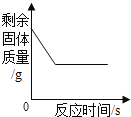
(4)为确定实验结束后氧化铜是否已基本消耗完,请设完成下表中两种不同的方案。
操作 | 判断依据 | 结论 | |
方案一 | 玻璃管中固体取样,加稀盐酸 | 现象:_______ | CuO已消耗完 |
方案二 | 称量玻璃管中残留固体质量 | 固体质量为____g |