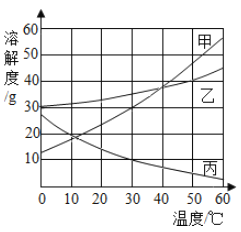
题目内容
【题目】海水晒粗盐的主要成分是NaCl,如图是除去粗盐中MgCl2、Na2SO4、CaCl2等杂质的流程图。
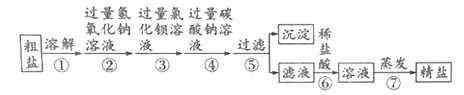
(1)以上操作中发生反应中有NaCl生成的反应有几个?________________________
(2)写出操作②中发生的化学反应方程式。____________________
(3)某同学向操作⑥后所得的溶液中滴加无色酚酞溶液,无明显现象,请设计实验方案证明该溶液中所含溶质的成分。(写出实验步骤、现象和结论)_________________
【答案】6 MgCl2+2NaOH═Mg(OH)2↓+2NaCl 取操作⑥后所得的溶液于试管中,加入适量碳酸钠,有气泡产生,证明含有盐酸(合理即可)
【解析】
(1)加入过量的NaOH溶液,反应的化学方程式为:MgCl2+2NaOH═Mg(OH)2↓+2NaCl;加入过量的BaCl2溶液,反应的化学方程式为:Na2SO4+BaCl2═BaSO4↓+2NaCl;加入过量的Na2CO3溶液,反应的化学方程式为:BaCl2+Na2CO3═BaCO3↓+2NaCl、CaCl2+Na2CO3═CaCO3↓+2NaCl;向滤液中加入盐酸,反应的化学方程式为:Na2CO3+2HCl═2NaCl+CO2+H2O、NaOH+HCl═NaCl+H2O;综上所述一共发生6个反应;
(2)由(1)可知操作②中发生的化学反应方程式为:MgCl2+2NaOH═Mg(OH)2↓+2NaCl;
(3)Na2CO3、NaOH都显碱性,向操作⑥后所得的溶液中滴加无色酚酞溶液,无明显现象,说明溶液中没有Na2CO3和NaOH;可能含有氯化氢,可利用碳酸钠与之反应产生气泡检验,方案如下:取操作⑥后所得的溶液于试管中,加入适量碳酸钠,有气泡产生,证明含有盐酸(合理即可)。

【题目】小明的大爷是种植蔬菜专业户,去年购买的化肥,由于外装上的字迹看不清,只记得是硫酸钾、碳酸氢铵、氯化铵中的一种,大爷正为此烦恼。
(1)小明利用学过的化学知识,设计了如下实验方案帮助鉴别化肥。
实验步骤 | 实验现象 | 实验结论 |
取上述化肥少量于一容器中,加入少量熟石灰粉末,混合研磨 | 嗅到_____。 | 该化肥不是硫酸钾 |
(2)小明假期到农田施肥时,发现撒落在地上的碳酸氢铵在阳光的照射下很快会消失,同时闻到浓烈的刺激性气味。他很好奇,返校后和同学们进行探究,请你一同参与:
(提出问题)温度较高时,碳酸氢铵能分解吗?产物是什么?
(猜想与假设)碳酸氢铵受热易分解,产物可能为水、二氧化碳、氨气。
收集资料:氨气能使湿润的红色石蕊试纸变蓝。
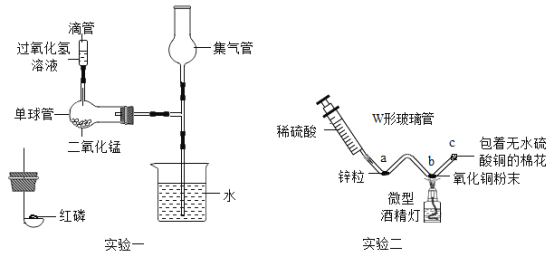
实验设计:小明设计了如图所示的装置进行实验(夹持仪器省略)。
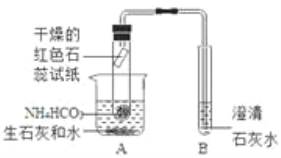
①根据现象:干燥的红色石蕊试纸变蓝,证明实验后生成了_____。
②装置B中澄清石灰水_____,证明产物中有二氧化碳生成,发生反应的化学方程式为_____。
③小红同学认为若将装置B中澄清石灰水改为NaOH溶液,再通过实验验证B中产物,也可以证明碳酸氢铵分解后有二氧化碳生成。
请你帮她设计并完成验证B中产物的实验:
实验步骤 | 实验现象 |
取装置B中溶液少许于试管中,滴加稀盐酸 | _____ |
(实验结论)碳酸氢铵受热易分解,写出反应的化学方程式_____。
(实验反思)根据以上实验,你认为碳酸氢铵化肥在存放时应注意的问题是_____(写一条)。通过探究找到了鉴别化肥的方法。
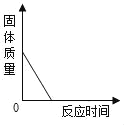
【题目】2018年5月18日我国第一艘国产航母试海成功,航母的许多电子元件使用了黄铜。为测定某黄铜(假设合金中仅含铜、锌)中铜的质量分数,兴趣小组同学称取20g黄铜粉末于烧杯中,将80g稀硫酸分四次加入,充分反应,测得实验数据如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量/g | 39.92 | 59.84 | 79.80 | 99.80 |
(1)黄铜粉末完全反应生成氢气的总质量为________g
(2)该黄铜中铜的质量分数为多少_______?(写出计算过程)
(3)第三次实验后所得溶液的溶质为__________。