题目内容
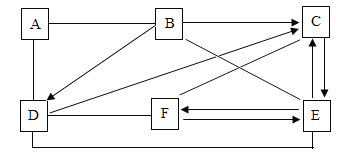
【题目】A-F为初中常见六种物质,它们之间的反应和全部转化关系如图所示。(“一”表示两种物质之间能发生反应,“→”表示一种物质能转化成另一种物质,省略部分反应物或生成物及反应条件,图中部分反应需要在溶液中进行,物质是溶液的只考虑溶质,且上述反应均在初中范围内),A为一种黑色固体单质,B有强烈的腐蚀性,且C、D、E、F为酸、碱、盐、氧化物中的一种。请回答下列问题:
(1)写出下列物质化学式A________;C_______;
(2)写出B→D化学方程式:_______;
(3)E→F的实验现象为:_______。
【答案】Fe CO2 ![]() 无色溶液中产生白色沉淀
无色溶液中产生白色沉淀
【解析】
A-F为初中常见六种物质,A为一种黑色固体单质,B有强烈的腐蚀性,A、B会发生反应,铁粉是黑色固体,浓硫酸具有强烈的腐蚀性,A可能是铁,B可能是硫酸;B(硫酸)会转化成D,D会与铁反应,硫酸与氯化钡溶液反应生成硫酸钡和盐酸,铁与盐酸能发生反应, 则D可能是盐酸,且C、D、E、F为酸、碱、盐、氧化物中的一种,F会与D(盐酸)反应,盐酸能与氢氧化钠反应,则F是氢氧化钠,F(氢氧化钠)和E可以相互转化,氢氧化钠与二氧化碳反应生成碳酸钠和水,碳酸钠与氢氧化钙反应生成氢氧化钠和碳酸钙,则E是碳酸钠,C和E(碳酸钠)可以相互转化,氢氧化钠与二氧化碳反应生成碳酸钠和水,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,则C是二氧化碳。将猜想代入框图,猜想成立。
根据以上分析可知:
(1)物质化学式A是Fe;C是CO2。
(2)B→D的反应是硫酸与氯化钡溶液反应生成硫酸钡和盐酸,化学方程式为![]() 。
。
(3)E→F的的反应是碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,故实验现象为无色溶液中产生白色沉淀。

 快乐5加2金卷系列答案
快乐5加2金卷系列答案【题目】为探究化学反应前后物质的质量关系,设计如下实验方案:
实验原理:铁与硫酸铜溶液反应。
实验用品:①带胶塞的维形瓶;②托盘天平。
实验药品:①打磨好的铁钉;②装于试剂瓶内足量的硫酸钢溶液。
步骤Ⅰ:称量并记录相关物质的质量m1
步骤Ⅱ:将缺钉浸到硫酸铜溶液中,待有现象后,称量并记录相关物质的质量m2
(1)写出铁钉与硫酸铜溶液反应的化学方程式。______________
(2)步骤Ⅰ中,如何比较合理地称量到相关物质的质量m1?_______________________
(3)实验结束后,处理记录的相关数据。请你完成空白处的填写
仪器和用品 | 物质 | |
步骤Ⅰ中相关物质质量m1 | 带胶塞的锥形瓶 | 水、_______ |
步骤Ⅱ中相关物质质量m2 | 带胶塞的锥形瓶 | 水、_______ |
实验结论 | _______ | |