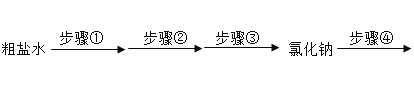
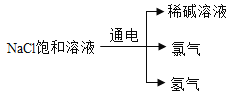
题目内容
【题目】实验室部分装置如图所示,请回答下列问题。
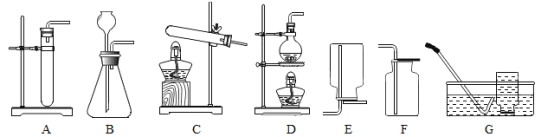
(1)①实验室用大理石和稀盐酸制备CO2的化学方程式为__________。
②用大理石和稀盐酸制备CO2时,能作为发生装置的是A或B,与A装置相比较,B装置的优点是便于在反应过程中________________________。
③选用F装置收集CO2时,验满方法是:____________________。则气体已满.
(2)若在实验室用C作为制备氧气的发生装置,可采用的药品是________________。并写出该反应的化学方程式_________________________________。
(3)选用G装置收集气体时,下列实验操作正确的是______________(填序号).
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中
②收集气体时,等到气泡连续且均匀放出,再将导管口移入集气瓶
③收满气体后,先将集气瓶移出水槽再盖上玻璃片
(4)实验室常用D装置来制备氯气(Cl2),推测其反应物可能是___________。(填序号).
①水和木炭 ②氯化钠固体和二氧化锰 ③浓盐酸和二氧化锰
【答案】CaCO3+2HCl=CaCl2+CO2↑+H2O 可随时添加液体药品; 取一个燃烧的木条放到集气瓶口,木条熄灭 氯酸钾与二氧化锰 2KClO3![]() 2KCl+3O2↑; ①② ③
2KCl+3O2↑; ①② ③
【解析】
(1)①实验室用大理石和稀盐酸制备CO2生成氯化钙二氧化碳和水,化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O故填:CaCO3+2HCl=CaCl2+CO2↑+H2O;
②B装置多了个长颈漏斗,在反应过程中可以随时添加液体药品,故填:可随时添加液体药品;
③二氧化碳不燃烧也不支持燃烧,取一个燃烧的木条放到集气瓶口,木条熄灭说明二氧化碳收集满了,故填:取一个燃烧的木条放到集气瓶口,木条熄灭;
(2)C装置适用于固体加热制取氧气,且试管口没有放棉花团,所以是加热氯酸钾与二氧化
锰的混合物制取氧气,故填:氯酸钾与二氧化锰; 2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(3)反应前,应将集气瓶装满水,用玻璃片盖住瓶口,倒立在盛水的水槽中;收集气体
时,观察到水中导管口有气泡均匀连续冒出时,开始收集气体;待集气瓶里的水排完后,在水面下用玻璃片盖住瓶口,再移出水槽;故选:①②;
(4)装置D适用于固体与液体在加热的条件下反应,因①中不含氯元素,②是两种固体,③中既含氯元素,又是固体与液体之间发生的反应,故选:③。

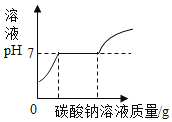
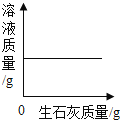
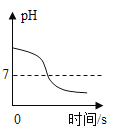
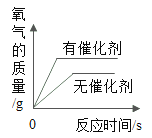
【题目】常温下,往盛放适量M物质的烧杯中逐渐加入N物质并充分搅拌,下图横坐标x表示N物质的质量,纵坐标y表示烧杯中的某物理量(见下表),下列实验与图像对应关系合理的是()

M | N | y | |
A | 水 | 浓硫酸 | 溶液的温度 |
B | 水 | 碳酸钠 | 溶液的pH |
C | 饱和氯化钠溶液 | 氯化钠 | 溶液的溶质质量分数 |
D | 硫酸铜溶液 | 铝粉 | 溶液质量 |
A.AB.BC.CD.D
【题目】金属的用途与性质密切相关。
(1)如图所示赤铁矿的主要成分是________(填名称);

(2)家用电线常用铜制,但在高压远距离输电中,常用铝代替铜,请根据信息分析,其原因是_______________;
铜 | 铝 | |
密度/(gcm-3) | 8.92 | 2.70 |
地壳中含量(质量分数/%) | 0.007 | 7.73 |
导电性(以银的导电性为100做标准) |
| |
(3)在空气中,铝具有很好的抗腐蚀性,其原因是______;
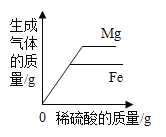
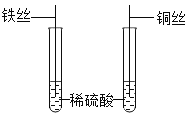
(4)为探究铁、铜的金属活动性,分别将铁丝、铜丝插入稀硫酸中(如图所示),说明铁比铜的金属活动性更强的实验现象是______,反应的化学方程式是______,后来,小贝选择两种药品,通过一步实验,也达到了实验目的,她选用的药品是 ____(写出一种药品组合即可);
(5)将一定质量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列有关说法正确的是____(填字母)。
A 若滤液为蓝色,则滤渣中一定有银,可能有铜
B 若滤渣中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、NO3﹣
C 若滤液为浅绿色,则滤渣中一定含银、铜、铝
D 若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+