题目内容
【题目】小亮同学对甲烷在氧气中燃烧后的气体产物的成分进行了相关探究(假定燃烧后产物均为氧化物)。
(知识回顾)
写出甲烷在足量的氧气中充分燃烧的化学方程式________________________________。
(实验探究)
小亮设计了下图装置进行实验探究(假定每步均完全反应)。
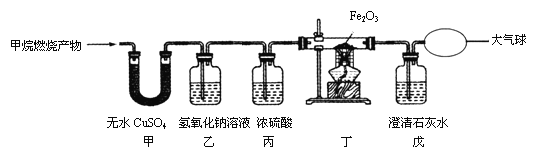
(1)完成实验报告:
实验操作 | 实验现象 | 实验结论 |
将燃烧后的气体 产物进行验证 | 甲中的白色固体变蓝 | 燃烧产物中有_______ |
乙装置质量增加 | 燃烧产物中有CO2 | |
丁中玻璃管内________; 戊中________ | 燃烧产物中有CO |
(2)写出丁中玻璃管内发生反应的化学方程式______________。
(拓展延伸)
实验结束,对相关装置进行称量(忽略空气成分对实验的干扰):甲装置增重5.4g,乙装置增重4.4g。
(1)根据以上数据,写出该实验中甲烷燃烧的化学方程式______________。
(2)若使上述实验中的甲烷充分燃烧,则理论上至少还需要氧气的质量为______________。
(交流与反思)
下列有关家庭使用天然气(主要成分为甲烷)的说法,正确的是___________。
A 天然气无毒,但是燃烧不充分产生CO会使人中毒,因此使用时需要良好的通风
B 天然气如果燃烧不充分,产生的热量会减少,从而浪费了资源
C 天然气泄漏报警器应安装在距地面约0.3米处
D 夜间若发现天然气泄漏,应立即开灯关闭阀门,并打开排气扇
【答案】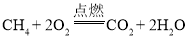 H2O(或水) 红色固体变成黑色固体 澄清石灰水变浑浊
H2O(或水) 红色固体变成黑色固体 澄清石灰水变浑浊 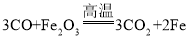
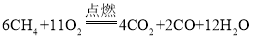 0.8g AB
0.8g AB
【解析】
知识回顾:
甲烷在足量的氧气中充分燃烧生成水和二氧化碳,反应的化学方程式为: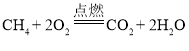
(1)甲中的白色固体变蓝,说明反应生成了水;乙装置质量增加,燃烧产物中有二氧化碳,二氧化碳和氢氧化钠反应生成了碳酸钠;丁中玻璃管内红棕色固体变成黑色固体,戊中澄清石灰水变浑浊,说明氧化铁和一氧化碳反应生成了铁和二氧化碳,进一步说明燃烧产物中有一氧化碳;
(2)丁中玻璃管内氧化铁和一氧化碳反应生成铁和二氧化碳,发生反应的化学方程式为: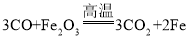 ;
;
拓展延伸:
(1)5.4g水中氢元素质量为:5.4g×![]() =0.6g,甲烷质量为:0.6g÷
=0.6g,甲烷质量为:0.6g÷![]() =2.4g,甲烷中碳元素质量为:2.4g-0.6g=1.8g,二氧化碳中碳元素质量为:4.4g×
=2.4g,甲烷中碳元素质量为:2.4g-0.6g=1.8g,二氧化碳中碳元素质量为:4.4g×![]() =1.2g,一氧化碳中碳元素质量为:1.8g-1.2g=0.6g,一氧化碳质量为:0.6g÷
=1.2g,一氧化碳中碳元素质量为:1.8g-1.2g=0.6g,一氧化碳质量为:0.6g÷![]() =1.4g,参加反应的氧气质量为:4.4g+5.4g+1.4g-2.4g=8.8g,
=1.4g,参加反应的氧气质量为:4.4g+5.4g+1.4g-2.4g=8.8g,
甲烷、氧气、二氧化碳、一氧化碳、水的化学计量数之比为:![]() :
:![]() :
:![]() :
:![]() :
:![]() =6:11:4:2:12,因此甲烷燃烧的化学方程式为:
=6:11:4:2:12,因此甲烷燃烧的化学方程式为: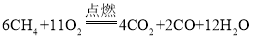 。
。
(2)设2.4g甲烷充分燃烧需要氧气质量为x,

![]() ,
,
解得x=9.6g,
答:若使上述实验中的甲烷充分燃烧,则理论上至少还需要氧气的质量为:9.6g-8.8g=0.8g。
交流与反思:
A、天然气无毒,但是燃烧不充分产生CO会使人中毒,因此使用时需要良好的通风,该选项正确;
B、天然气如果燃烧不充分,产生的热量会减少,从而浪费了资源,该选项正确;
C.甲烷密度比空气小,因此天然气泄漏报警器应安装在高处,该选项错误;
D.夜间若发现天然气泄漏,不能开灯、也不能打开排气扇,这是因为打开时会产生电火花,可能发生爆炸,该选项错误。故AB。